Anotace předmětu:
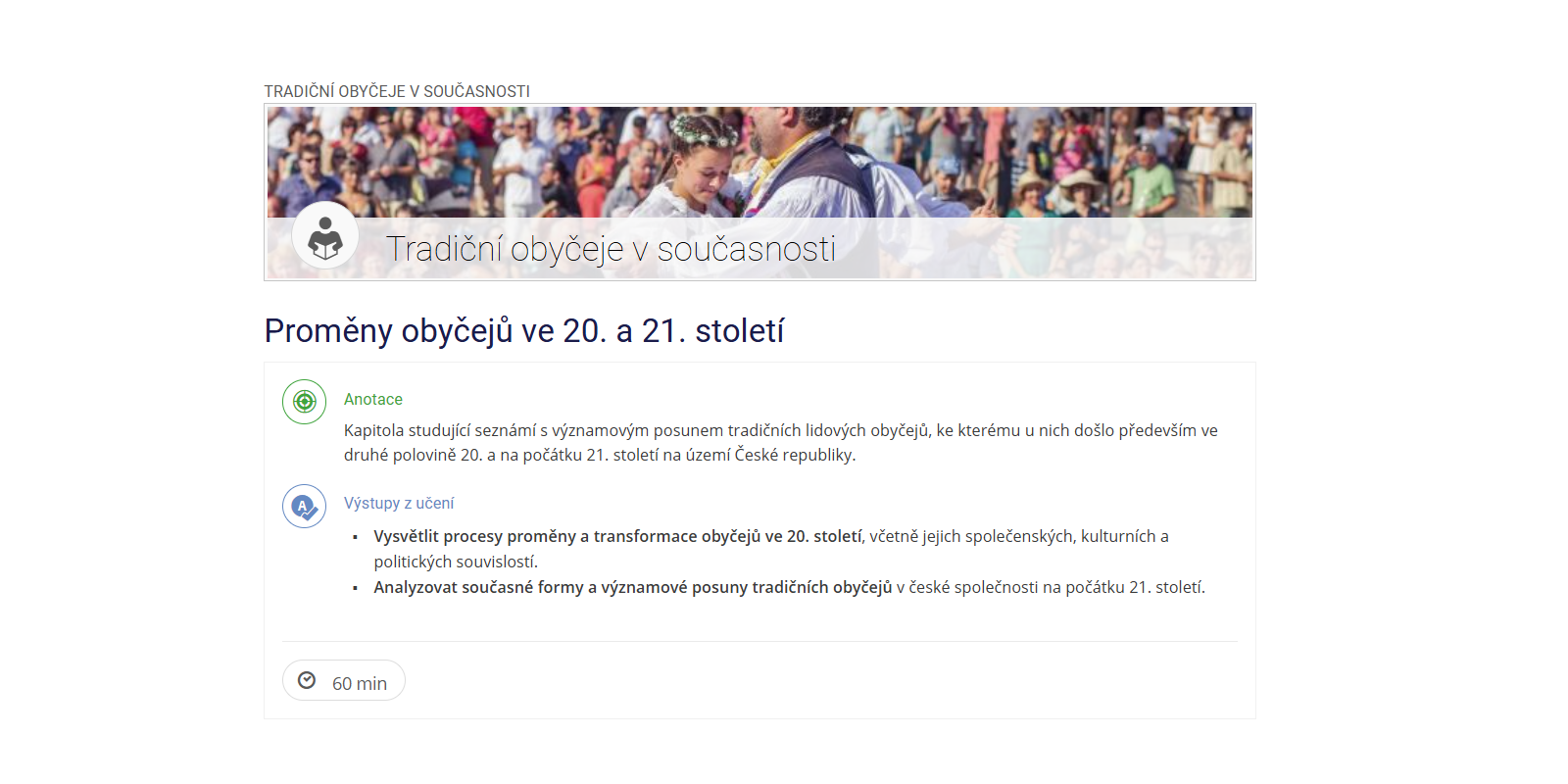
Předmět je koncipován jako teoreticko-praktický. Seznamuje studenty se základy biofyziky a jejím využitím v oblasti medicínských diagnostických a léčebných metod. Studenti získají základní informace o fyzikálních odlišnostech jednotlivých metod a jejich biologických účincích. Seznámí se s jednotlivými druhy těchto metod a přístroji, kterými jsou tato vyšetření prováděna.
Kapitoly:
-
1.1 Elementární částice, formy hmoty
-
1.2 Energie
-
1.3 Kvantové jevy
-
1.4 Atom vodíku spektrum
-
1.5 Struktura elektronového obalu těžších atomů
-
1.6 Excitace, emise a ionizace, vazebná energie elektronu
-
1.7 Vlnově mechanický model atomu
-
1.8 Jádro atomu
-
1.9 Síly působící mezi atomy
-
1.10 Hmotnostní spektroskopie
Kapitola obsahuje:
13
Obrázek
1
Odpovědník
14
Text
Kapitola obsahuje:
14
Obrázek
1
Odpovědník
22
Text
Kapitola obsahuje:
12
Obrázek
1
Odpovědník
21
Text
Kapitola obsahuje:
19
Obrázek
1
Odpovědník
26
Text
Kapitola obsahuje:
13
Obrázek
1
Odpovědník
9
Text
Kapitola obsahuje:
17
Obrázek
1
Odpovědník
10
Text
Kapitola obsahuje:
21
Obrázek
1
Odpovědník
32
Text
Kapitola obsahuje:
3
Obrázek
1
Odpovědník
14
Text
Kapitola obsahuje:
9
Obrázek
1
Odpovědník
20
Text
Kapitola obsahuje:
1
Odpovědník
Předchozí