Máte zapnutý náhled celé osnovy, zpět na běžné zobrazení.
Načítání a prohlížení osnovy může být v závislosti na množství obsahu pomalejší.
Fyziologie

-
4.1 Přehled fyziologie dýchání
-
4.2 Hlavní procesy dýchání
-
4.3 Krevní plyny
-
4.4 Respirace a acidobazická rovnováha
-
4.5 Regulace dýchání
-
4.6 Obranné dýchací reflexy
-
4.7 Hypoxie
-
4.8 Hypokapnie a hyperkapnie
-
4.9 Poruchy respiračních funkcí
-
4.10 Patofyziologie hlavních onemocnění plic
-
4.11 Respirační insuficience
-
6.1 Přehled a základní pojmy z fyziologie trávicího ústrojí
-
6.2 Řízení trávicího systému
-
6.3 Pohyby trávicí trubice
-
6.4 Principy trávení a vstřebávání
-
6.5 Imunitní systém trávicího ústrojí
-
6.6 Krevní oběh trávicího ústrojí
-
6.7 Dutina ústní
-
6.8 Hltan (farynx) a jícen (ezofagus)
-
6.9 Žaludek
-
6.10 Tenké střevo
-
6.11 Tlusté střevo a konečník
-
6.12 Slinivka břišní (pankreas)
-
6.13 Játra a žluč
-
6.14 Poruchy tvorby slin
-
6.15 Poruchy polykání (dysfagie)
-
6.16 Gastroezofageální reflux (GER)
-
6.17 Poruchy žaludeční motility a sekrece
-
6.18 Peptický vřed
-
6.19 Nevolnost a zvracení
-
6.20 Malabsorpční syndrom
-
6.21 Průjem a zácpa
-
6.22 Ileus
-
6.23 Nedostatečnost slinivky břišní (pankreatická insfucience)
-
13.1 Základní pojmy a principy
-
13.2 Hypotalamus-hypofýza
-
13.3 Žlázy regulované osou hypotalamus-hypofýza
-
13.4 Žlázy s odlišnou regulací
-
13.5 Další látky hormonálního charakteru
-
13.6 Základní pojmy
-
13.7 Patofyziologie jednotlivých žláz
-
13.7.1 Poruchy hypothalamu
-
13.7.2 Poruchy hypofýzy
-
13.7.3 Patofyziologie štítné žlázy
-
13.7.4 Patofyziologie kůry nadledvin
-
13.7.5 Patofyziologie pohlavních hormonů
-
13.7.6 Patofyziologie příštítných tělísek
-
13.7.7 Patofyziologie dřeně naledvin
-
13.7.8 Patofyziologie endokrinního pankreatu – diabetes mellitus
-
-
13.8 Testovací otázky
1 Základní fyziologické a patofyziologické principy a koncepty
1.1 Molekulární, buněčné a tkáňové základy fyziologie a patofyziologie
1.1.1 Buněčné transportní procesy
1. podle typu přenášeného iontu
- draslíkové
- sodíkové
- vápníkové aj.
2. podle mechanismu řízení – to znamená, jakým mechanismem je kanál otvírán.
- trvale otevřené
- řízené elektrickým napětím
- řízené chemicky (např. hormonem, mediátorem)
- řízené napětím i chemicky
- řízené mechanicky
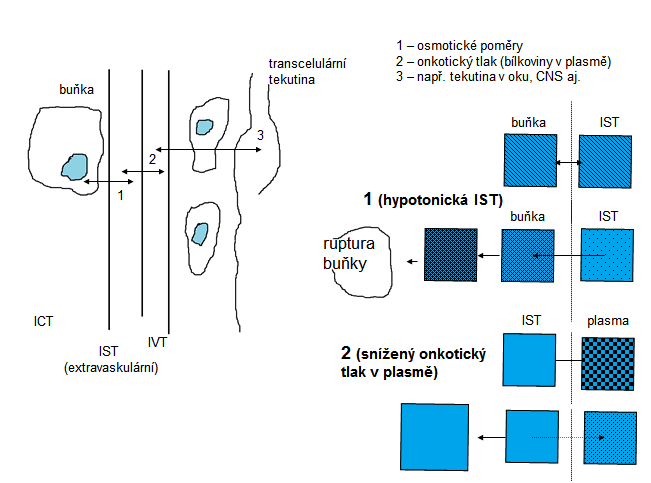
1.1.2 Přesuny tekutin
1.1.3 Rozložení iontů na membráně, elektrický membránový potenciál
Uvnitř buňky (intracelulárně) |
Vně buňky (extracelulárně) | |
Sodík (Na+) – mmol/l |
12 |
130 |
Draslík (K+) – mmol/l |
150 |
4 |
Vápník (Ca+) – mmol/l |
10-5 až 10-4 |
2,5 |
Chlorid (Cl-) – mmol/l |
4 |
110 |
Bikarbonáty (HCO3-) – mmol/l |
8 |
30 |
Bílkoviny_ – mmol/l |
155 |
1.1.4 Buněčná komunikace
1.1.5 Buněčné dělení a buněčná smrt
1.1.6 Geny, genová exprese
1.2 Regulace ve fyziologii
1.3 Základní pojmy v patofyziologii
2 Fyziologie a patofyziologie krve
2.11 Testovací otázky
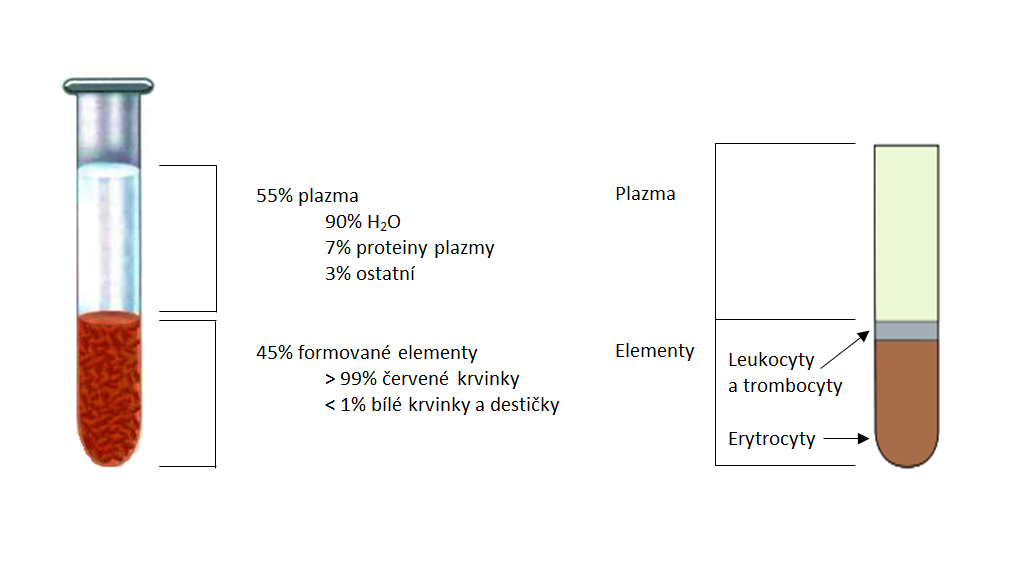
2.1 Složení krve
2.1.1 Plazma
2.1.2 Červené krvinky
2.1.3 Bílé krvinky
2.1.4 Krevní destičky
2.2 Funkce krve
2.3 Tvorba krve
2.4 Zástava krvácení a krevní srážení
2.5 Krevní skupiny
2.6 Anémie a polycytémie
Faktor tvorby červených krvinek |
Druh anémie |
Obv. typ anémie |
Kostní dřeň |
Aplastická anémie |
Normocytární, normochromní |
Erytropoetin |
Anémie při selhání ledvin |
Normocytární, normochromní |
Železo |
Anémie z nedostatku železa |
Mikrocytární, hypochromní |
Vitamin B12 a listová kyselina |
Megaloblastová anémie |
Makrocytární, hyperchromní |
Zánět |
Anémie chronických chorob |
Obv. normocytární, normochromní |
2.7 Nedostatek a nadbytek bílých krvinek
2.8 Leukémie
2.9 Krvácivé stavy
2.10 Trombóza
3 Fyziologie a patofyziologie imunity
3.11 Testovací otázky
3.1 Imunitní systém
3.2 Hlavní buňky imunitního systému
Granulocyty jsou další skupinou bílých krvinek. Neutrofilní granulocyty jsou zejména fagocytující buňky, účastní se zánětu, mohou být i zdrojem poškození, protože obsahují četné enzymy, které likvidují pohlcené mikroorganismy, ale za určitých okolností mohou poškodit vlastní tkáň. Eozinofilní a čátečně též bazofilní granulocyty se podílejí zejm. na alergických reakcích.
3.3 Hlavní histokompatibilní systém
3.4 Cytokiny
3.5 Imunita nespecifická
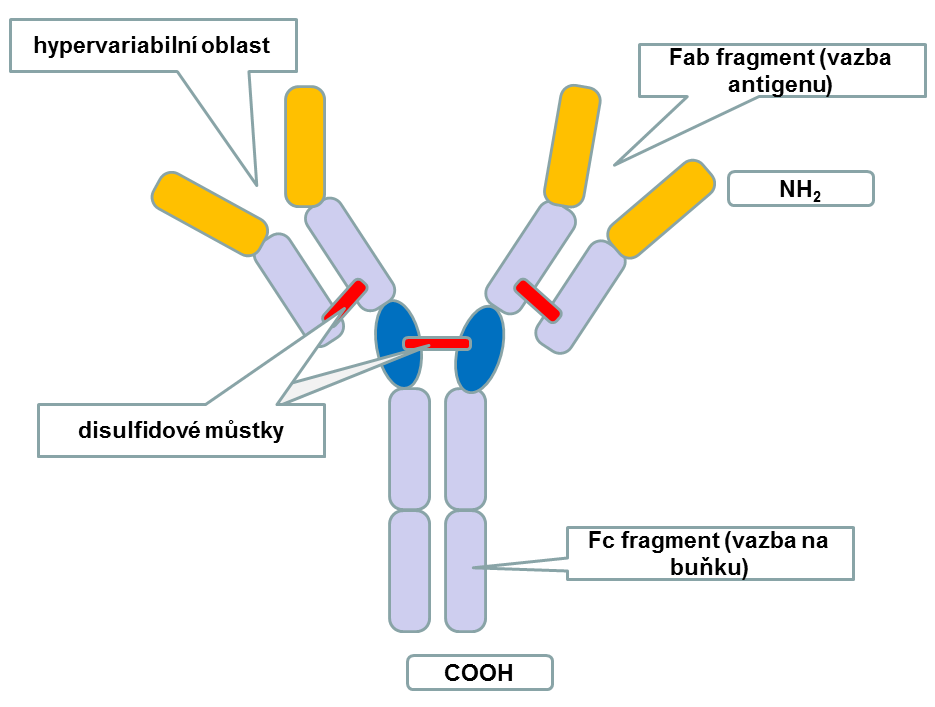
3.6 Imunita specifická
3.7 Imunopatologické reakce
3.8 Alergie
Alergie je chorobný stav, který vzniká přecitlivělou reakcí imunitního systému na jinak běžné antigeny v okolí (pyl, prach, roztoči, zvířecí chlupy, různé chemické látky, léky). Vzniká z důvodu nepřiměřené reakce imunitního systému na běžný („bezpečný“) antigen okolního prostředí, který se v tomto případě často označuje jako alergen. Alergeny se do těla dostávají vdechnutím, potravou, či kontaktem. Může jít o pyly, exkrementy roztočů, některé potraviny, ale i kovy (např. nikl v náramku hodinek). V některých případech se malé molekuly, označované jako hapten mohou navázat na větší molekulu, čímž vznikne nová antigenní struktura.
Při vzniku alergických nemocí se uplatňují popsané imunopatologické reakce. Nejvýznamnější skupinu alergiků tvoří atopici. Jde o osoby s náchylností k reakcí I. typu, často s familiárním výskytem. K hlavním projevům atopie patří atopický ekzém, asthma bronchiale, senná rýma; dále bývá kopřivka, zánět spojivek apod.
Klasickou alergií jsou atopie (imunopatologická reakce I. typu s časnou přecitlivělostí). Tzn. že projevy včetně život ohrožujících mohou vznikat velmi rychle. U senzibilizovaného jedince dochází k alergické reakci krátce po kontaktu s alergenem a má buď projevy lokalizované do určitého orgánu (místní projevy, např. senná rýma či kopřivka), nebo má celkovou reakci (anafylaktický šok). Akutní fáze vzniká několik minut po kontaktu s alergenem, vyplavuje se masivně histamin a další látky, rozšiřují se cévy, zvyšuje se jejich propustnost, mohou se zúžit průdušky atd. Po této fázi nastupuje cca do 12 hodin pozdní fáze, je méně dramatická, ale protože došlo k přilákání dalších buněk, objevují se známky zánětu a může dojít k trvalému poškozování tkání, což je nápadné např. u průduškového astmatu..
3.9 Autoimunita
3.10 Imunodeficience a imunosuprese
Po vstupu HIV do organismu dochází k fázi rychlého pomnožení s klinickými příznaky obdobnými chřipkovému onemocnění. Vzniká imunitní reakce a protilátky (ty lze využít k detekci a diagnostice infekce), virové částice jsou sice odstraněny z krevního oběhu, ale přetrvávají uvnitř imunitních buněk. Nastává různě dlouhé bezpříznakové období, během něhož může jedinec být stále infekční. Dochází k postupnému úbytku CD4+ T-lymfocytů, jejichž počet lze stanovit v krvi.
4 Fyziologie a patofyziologie dýchání
4.12 Testovací otázky
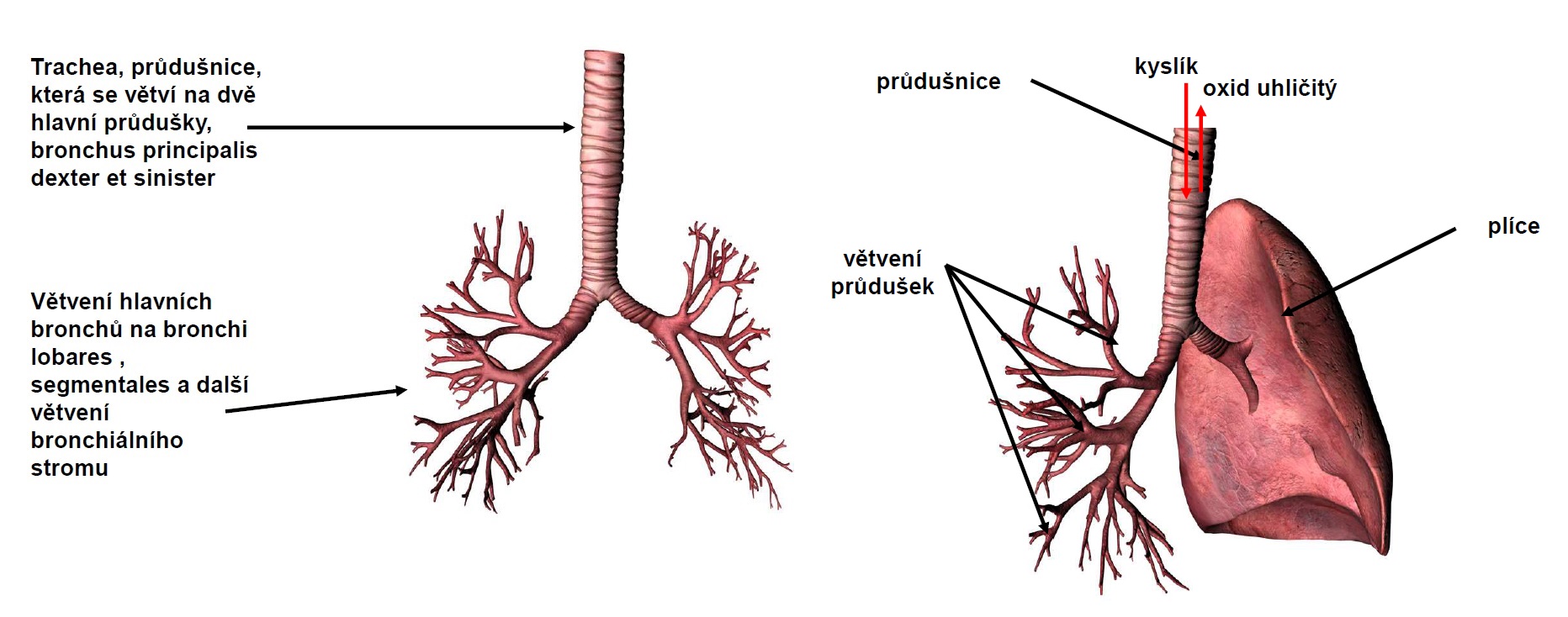
4.1 Přehled fyziologie dýchání
4.2 Hlavní procesy dýchání
Atmosférický vzduch |
Alveolární vzduch | |
Dusík |
596 (78 %) |
573 (74 %) |
Kyslík |
158 (21 %) |
100 (14 %) ↓ |
Oxid uhličitý |
0,3 (0,03 %) |
40 (5 %) ↑ |
Vodní páry |
5,7 (0,7 %) |
47 (6 %) ↑ |
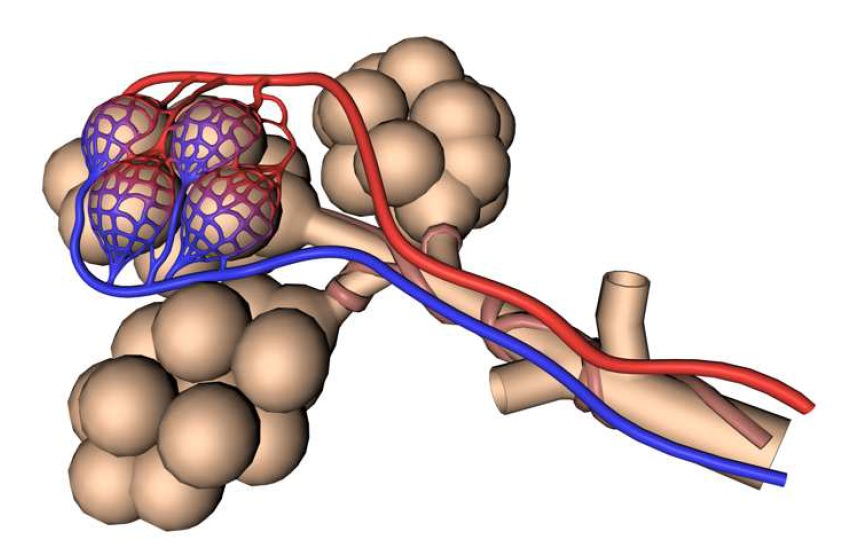
Arbor alveolaris s plicními alveoly obklopenými kapilárními sítěmi, ve kterých dochází k výměně plynů.
4.3 Krevní plyny
4.4 Respirace a acidobazická rovnováha
4.5 Regulace dýchání
4.6 Obranné dýchací reflexy
4.7 Hypoxie
4.8 Hypokapnie a hyperkapnie
4.9 Poruchy respiračních funkcí
4.10 Patofyziologie hlavních onemocnění plic
4.11 Respirační insuficience
5 Fyziologie a patofyziologie oběhu krve a lymfy
5.8 Testovací otázky
5.1 Přehled krevního a lymfatického oběhu
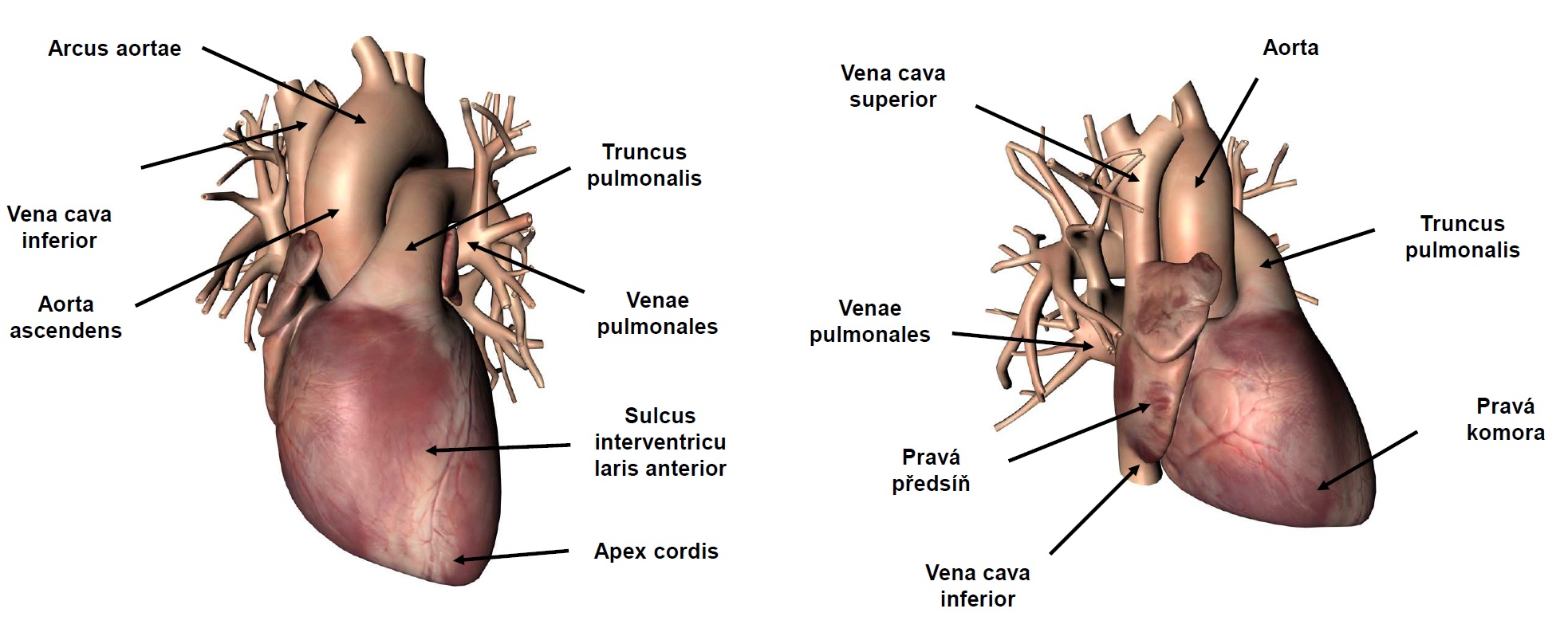
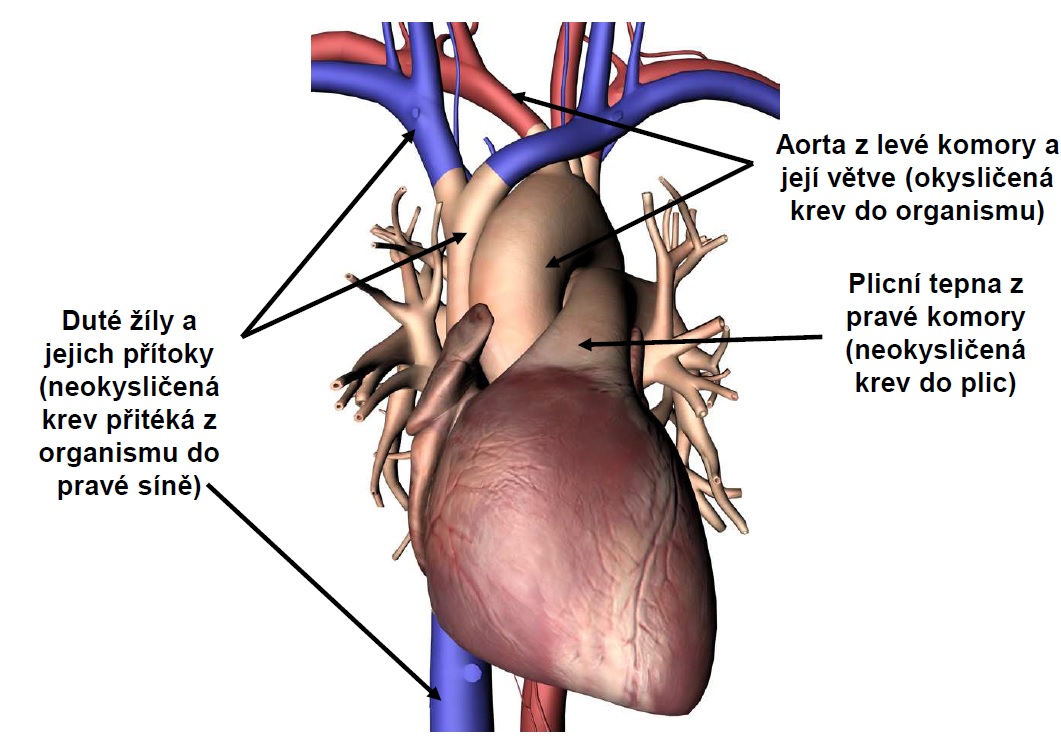
5.2 Srdce
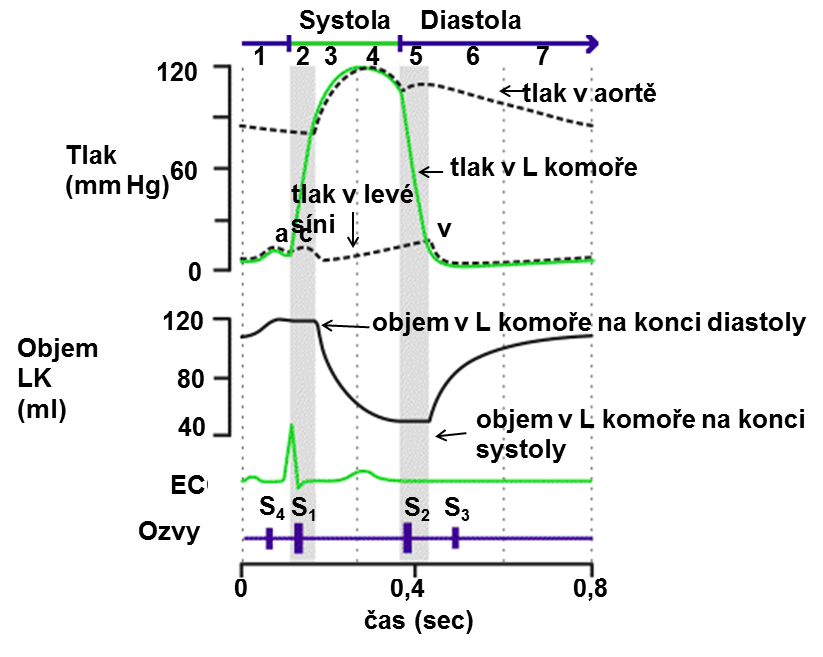
5.2.1 Srdce jako pumpa
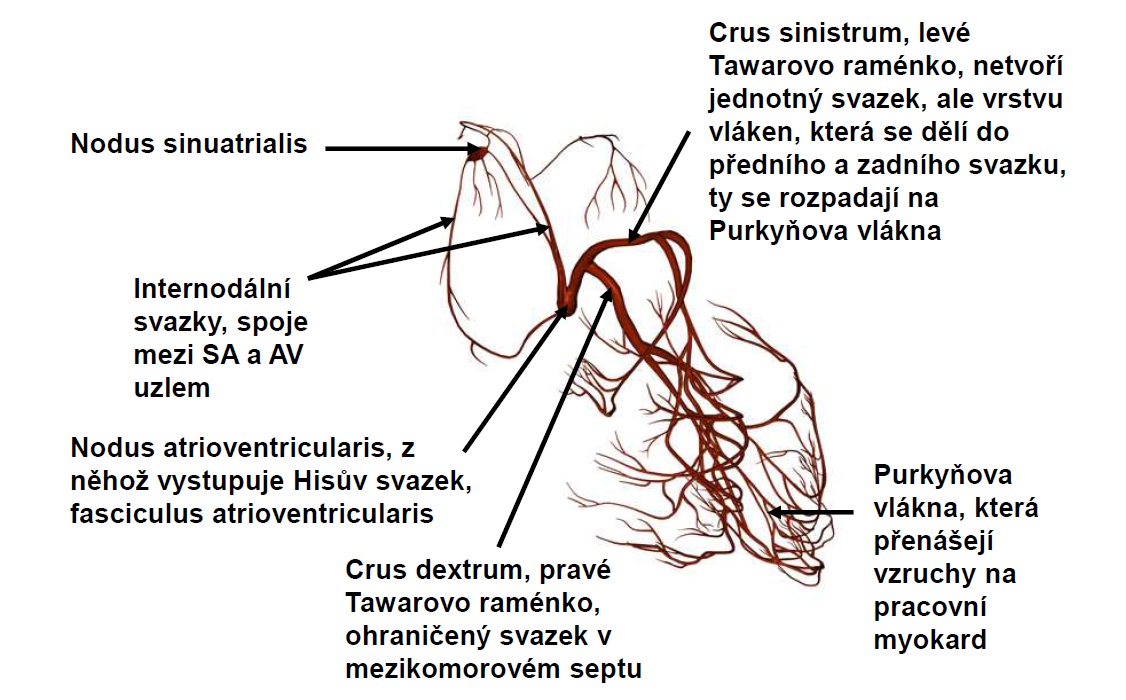
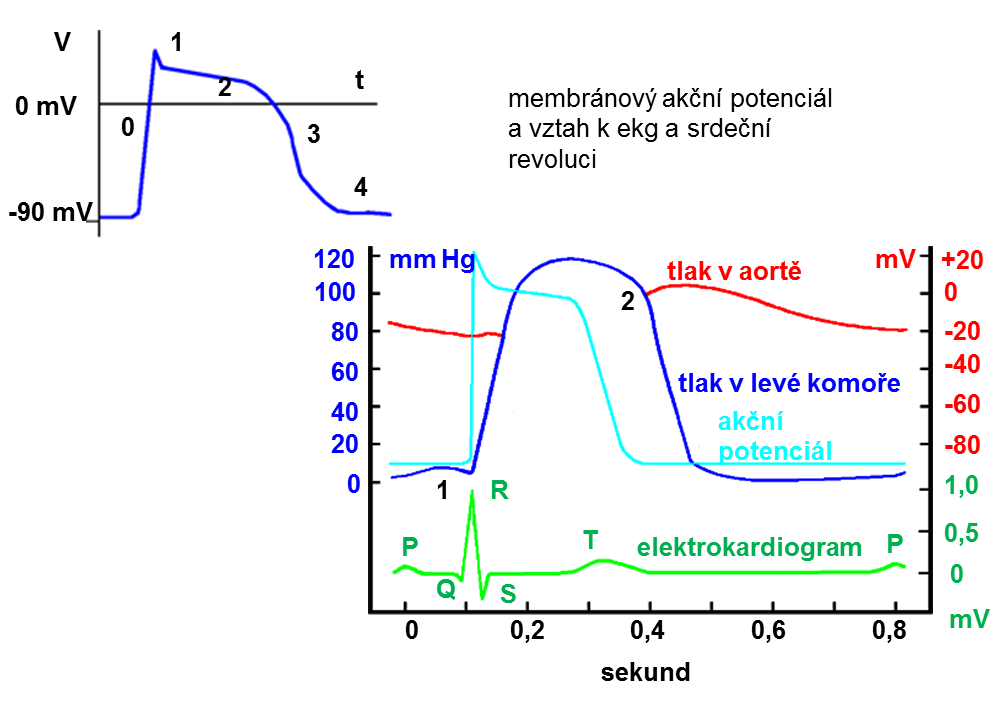
5.2.2 Elektrická činnost srdce
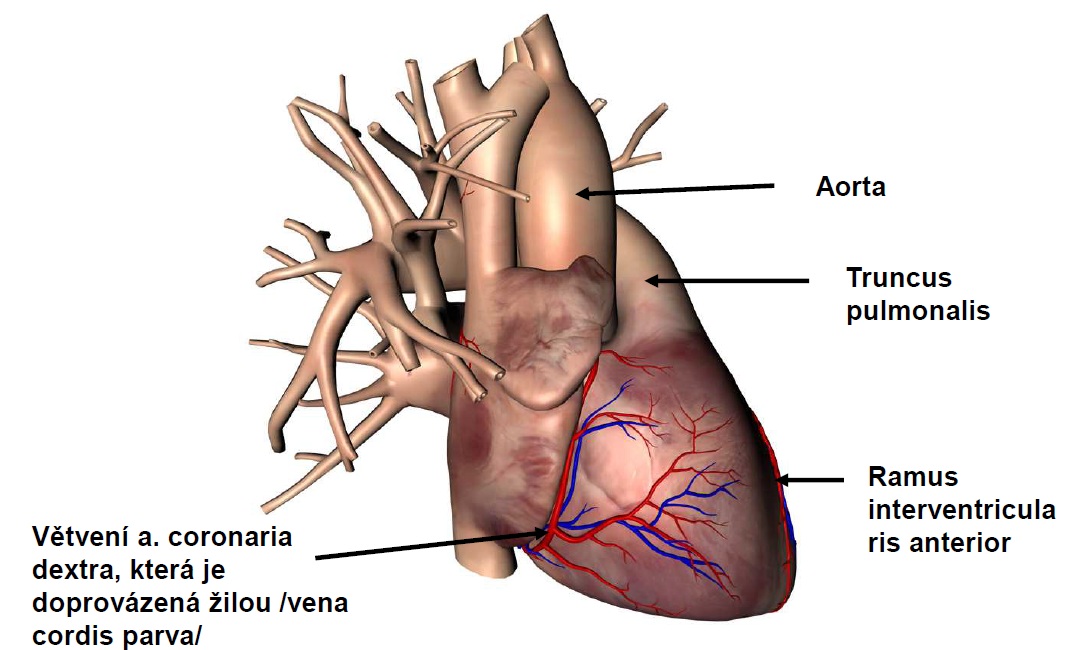
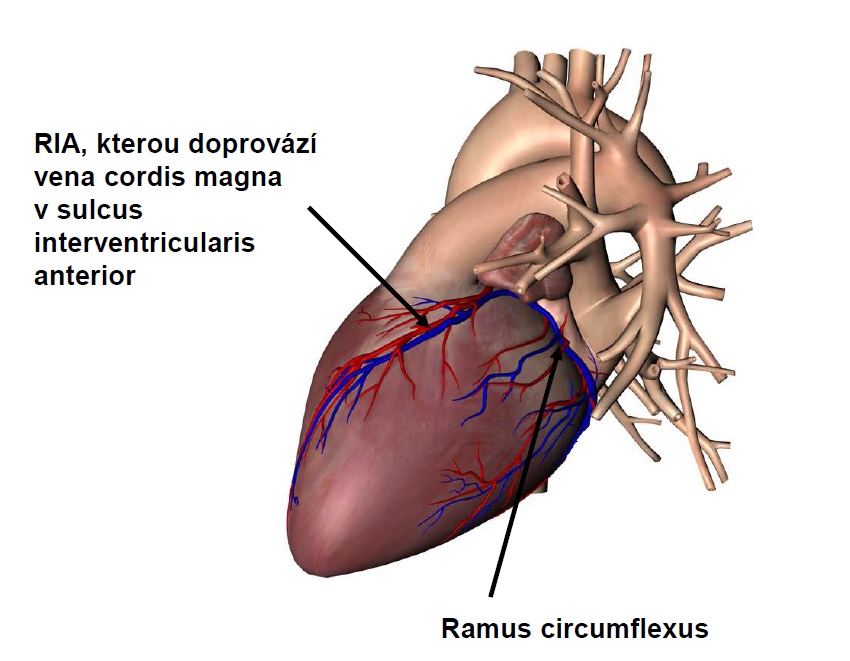
5.2.3 Krevní zásobení srdce a jeho metabolismus
Cévy a nervy srdce
Dělí se na ramus interventricularis anterior /RIA/ a ramus circumflexus.
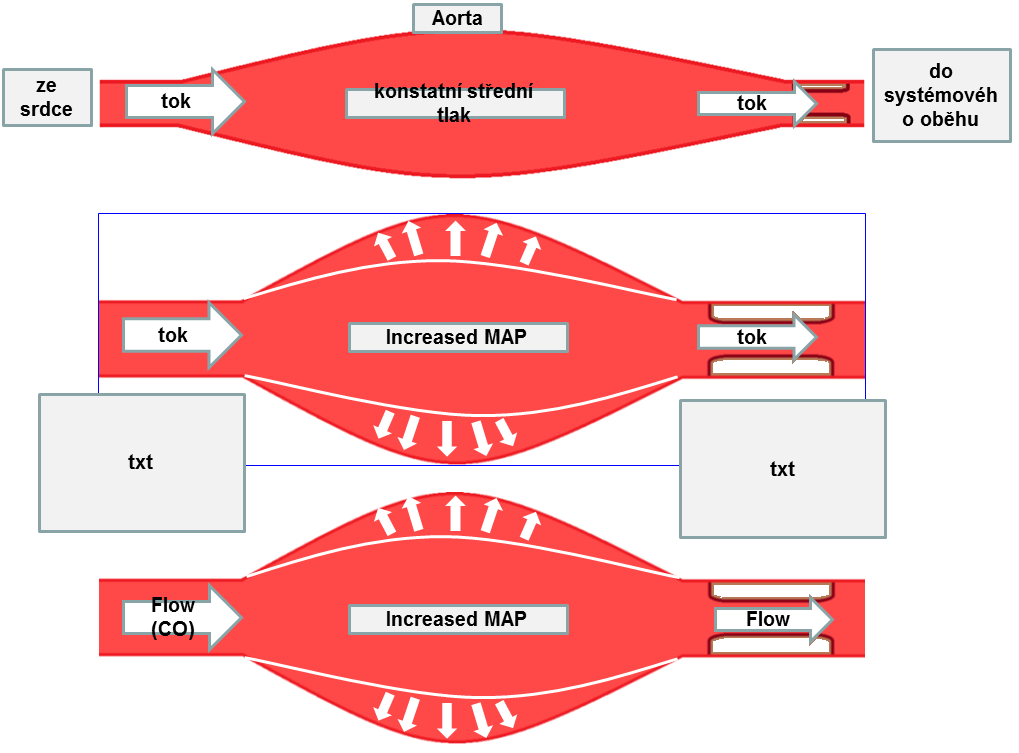
5.3 Tlak krve
Systolický TK je určen především srdečním stahem, množstvím krve, které srdce vypudí (tepovým objemem) a odporem, resp. poddajností aorty a velkých tepen během systoly, do nichž krev vypuzuje. Tyto cévy musí být dostatečně poddajné, aby množství krve pojaly; jsou-li málo poddajné (čili tuhé), systolický tlak se výrazně zvýší.
srdeční cyklus
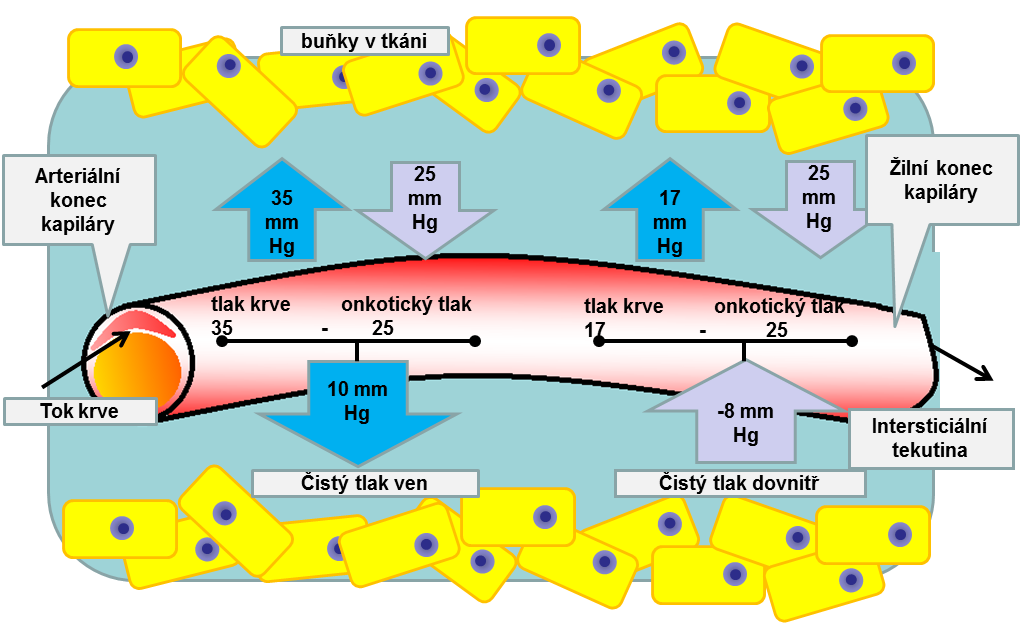
5.4 Fyziologie cév
Venózní (žilní) cirkulace
5.5 Speciální oblasti krevního oběhu
5.6 Regulace krevního oběhu
5.7 Patofyziologie krevního oběhu
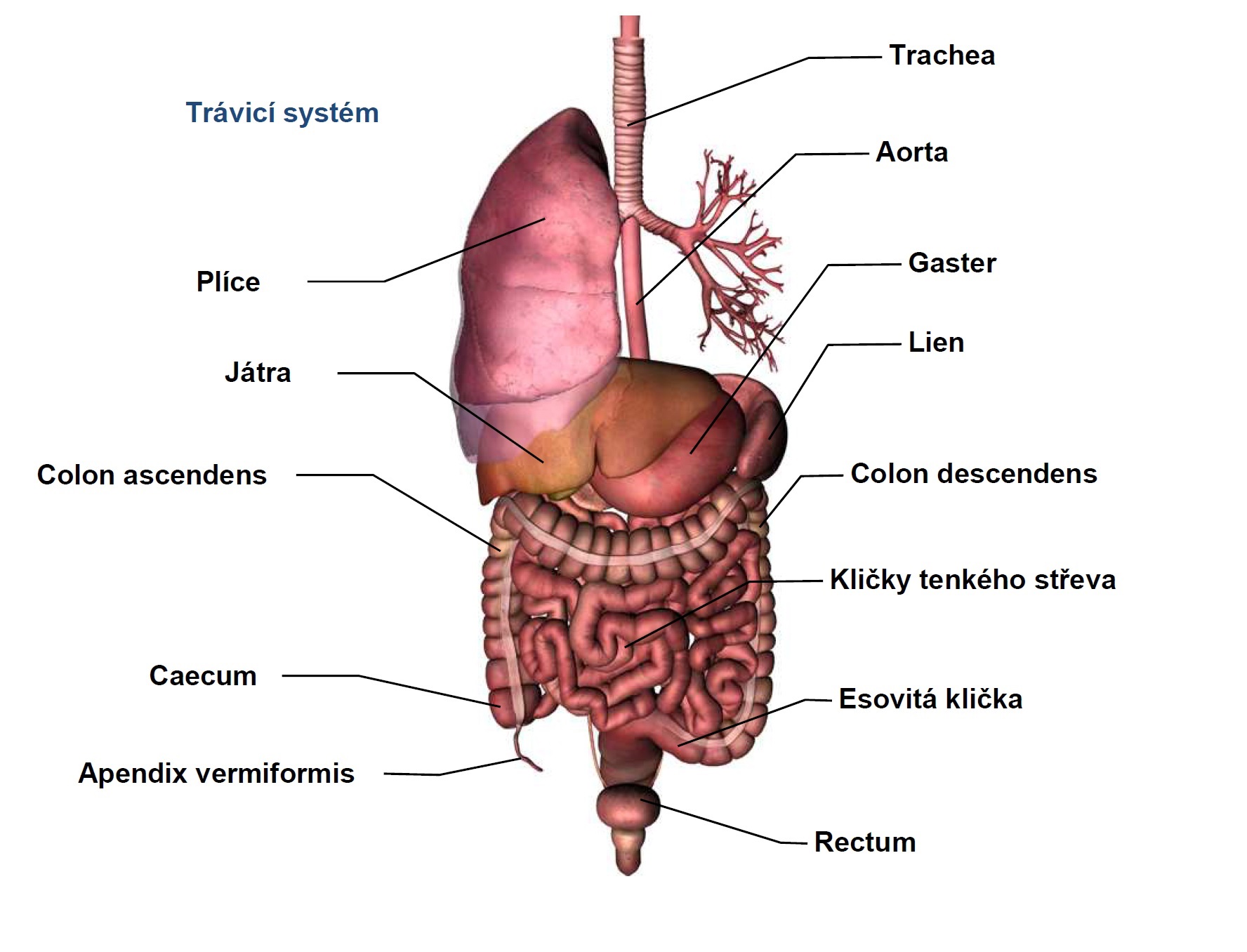
6 Fyziologie a patofyziologie trávení a vstřebávání
6.24 Testovací otázky
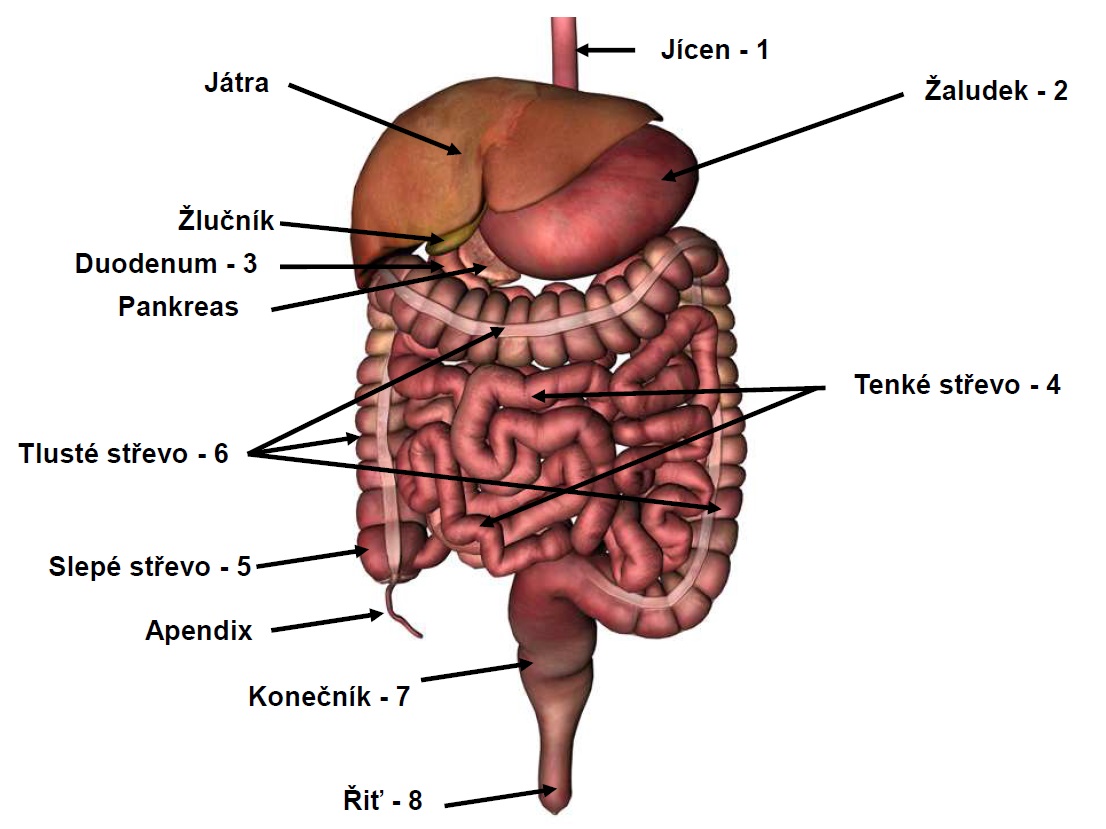
6.1 Přehled a základní pojmy z fyziologie trávicího ústrojí
6.2 Řízení trávicího systému
6.3 Pohyby trávicí trubice
6.4 Principy trávení a vstřebávání
6.5 Imunitní systém trávicího ústrojí
6.6 Krevní oběh trávicího ústrojí
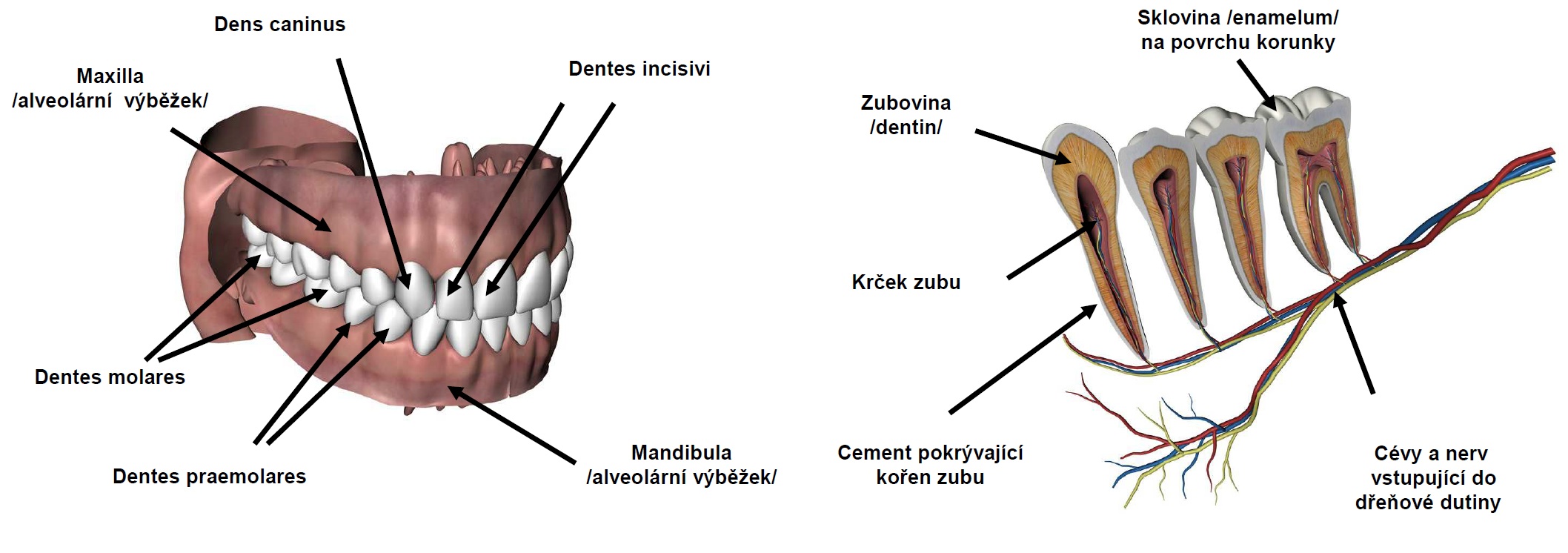
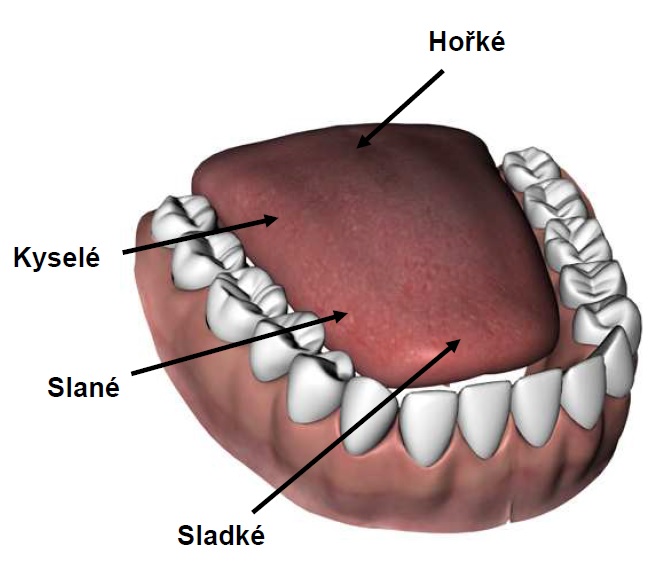
6.7 Dutina ústní
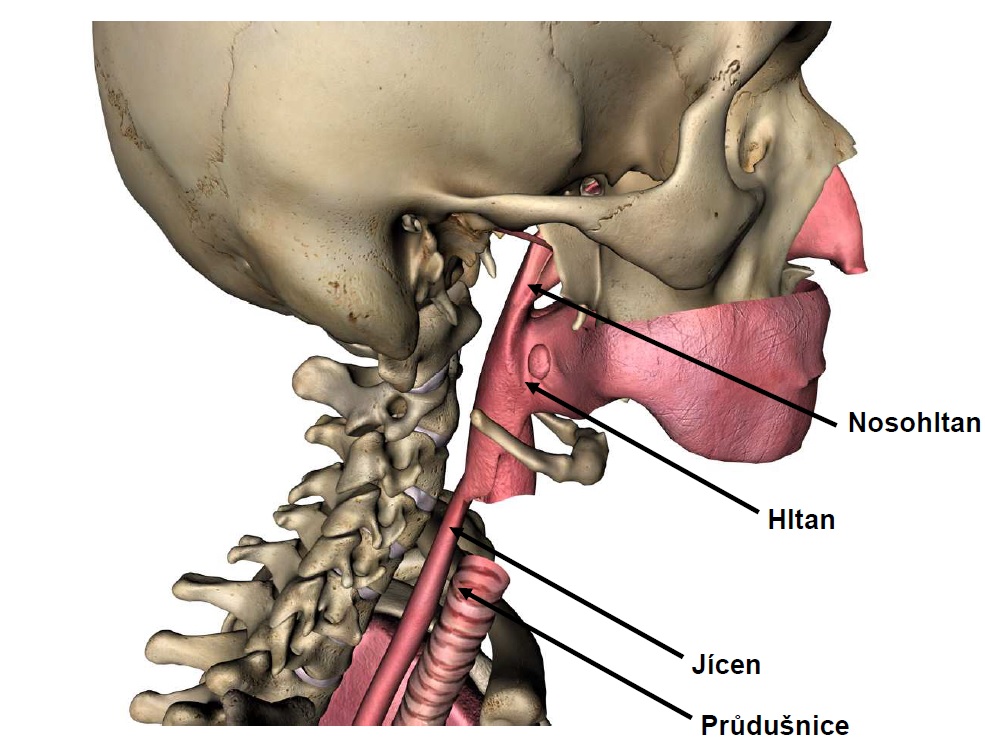
6.8 Hltan (farynx) a jícen (ezofagus)
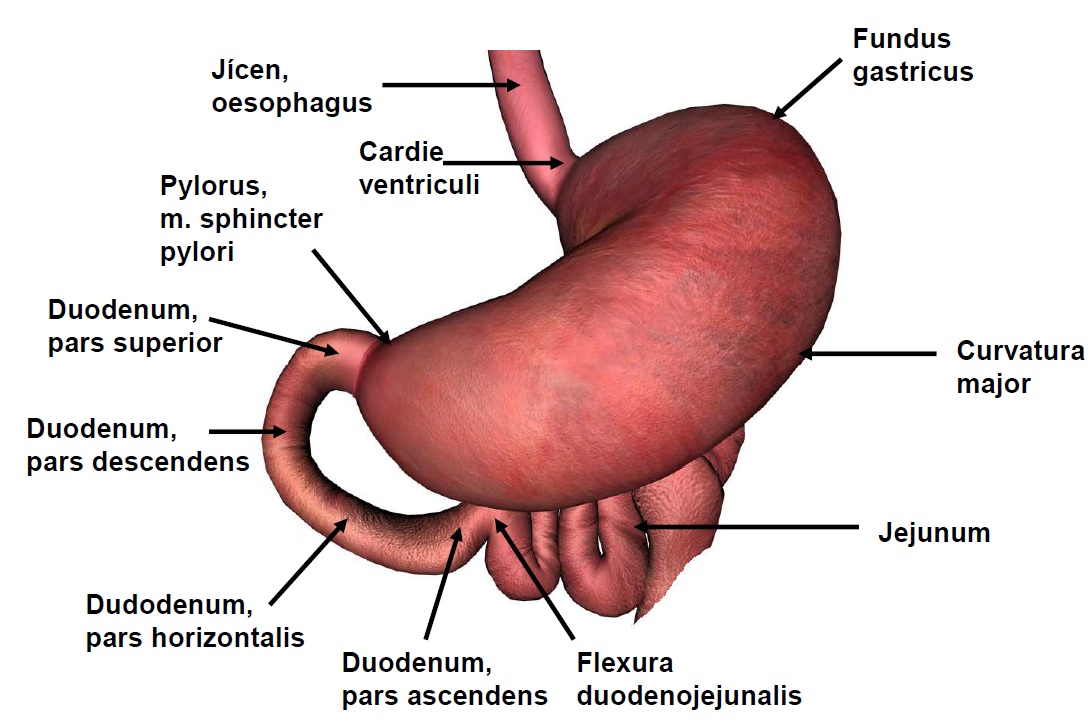
6.9 Žaludek
6.10 Tenké střevo
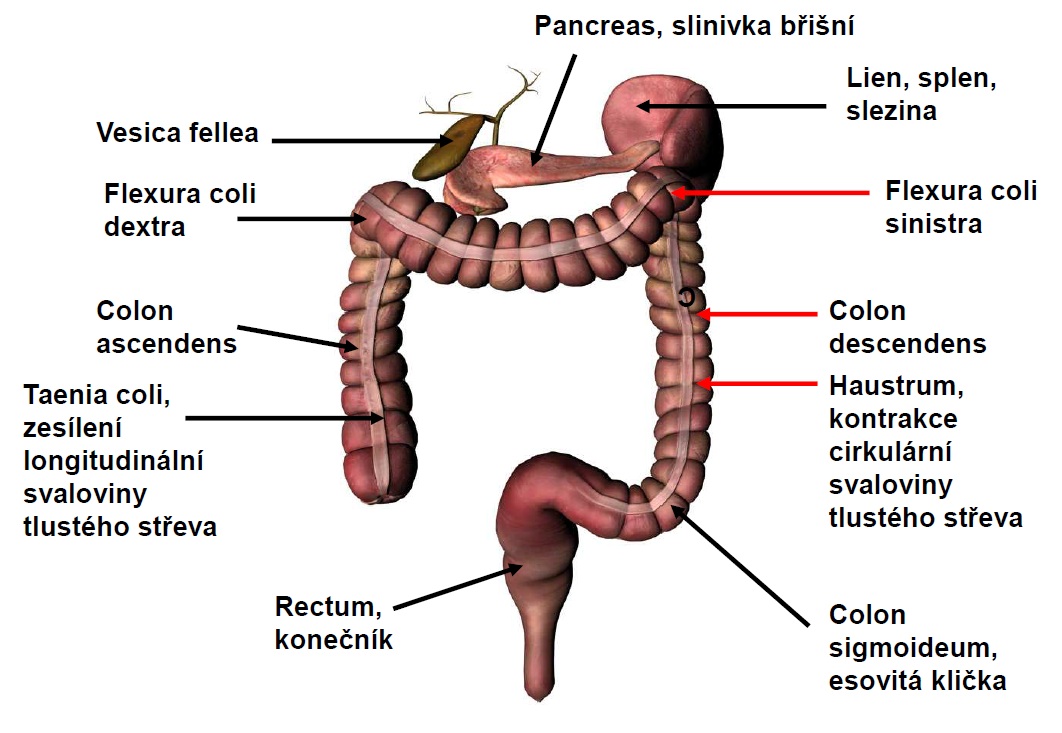
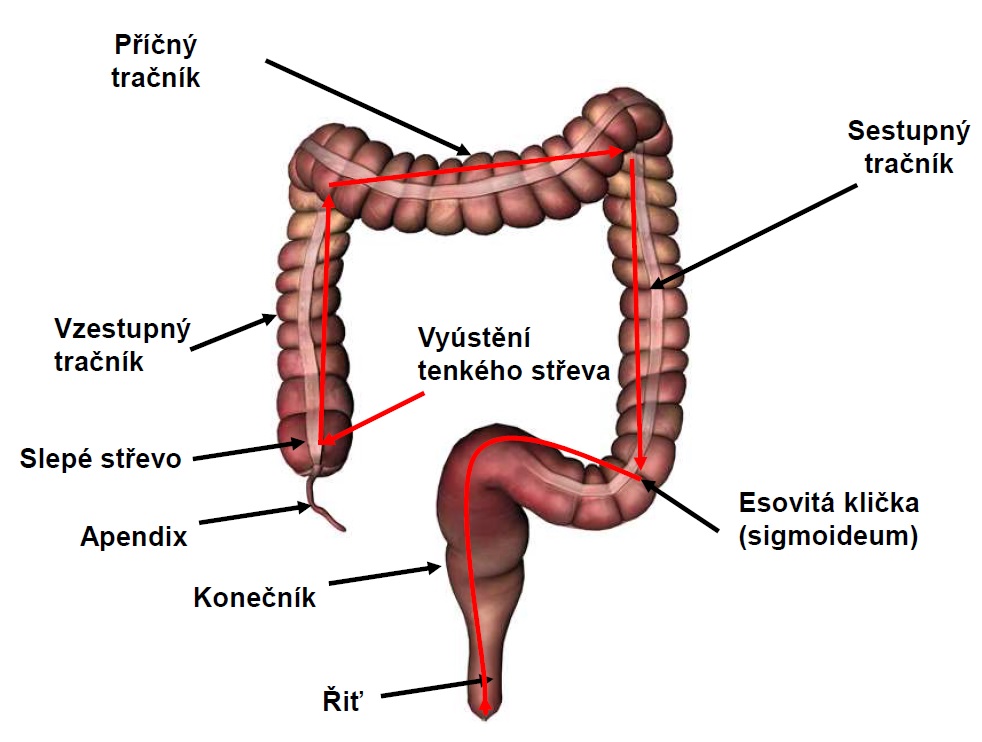
6.11 Tlusté střevo a konečník
6.12 Slinivka břišní (pankreas)
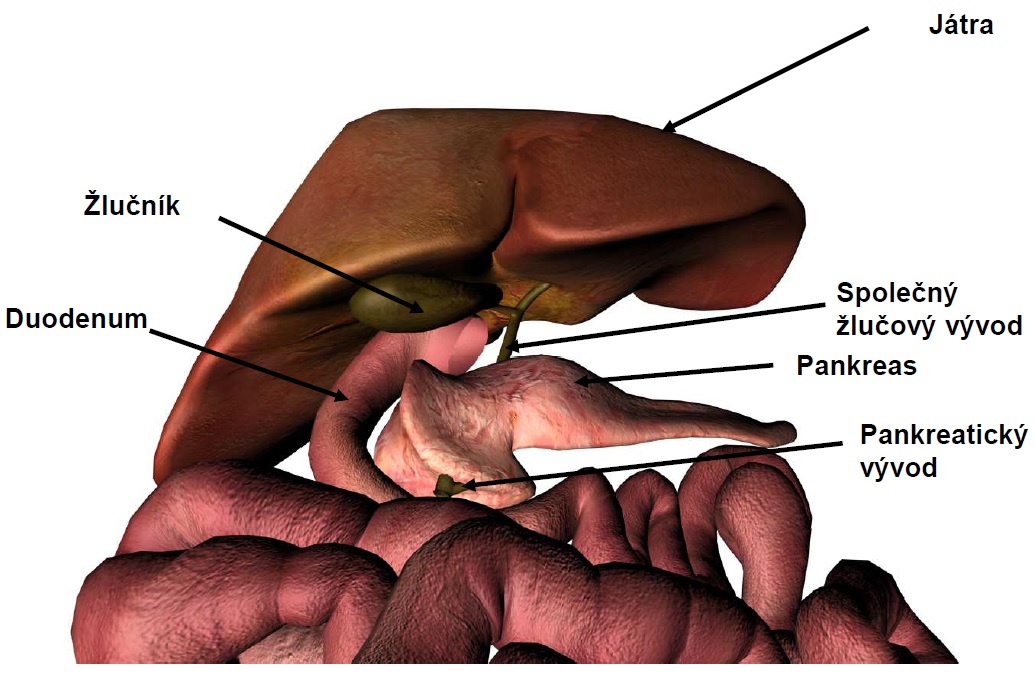
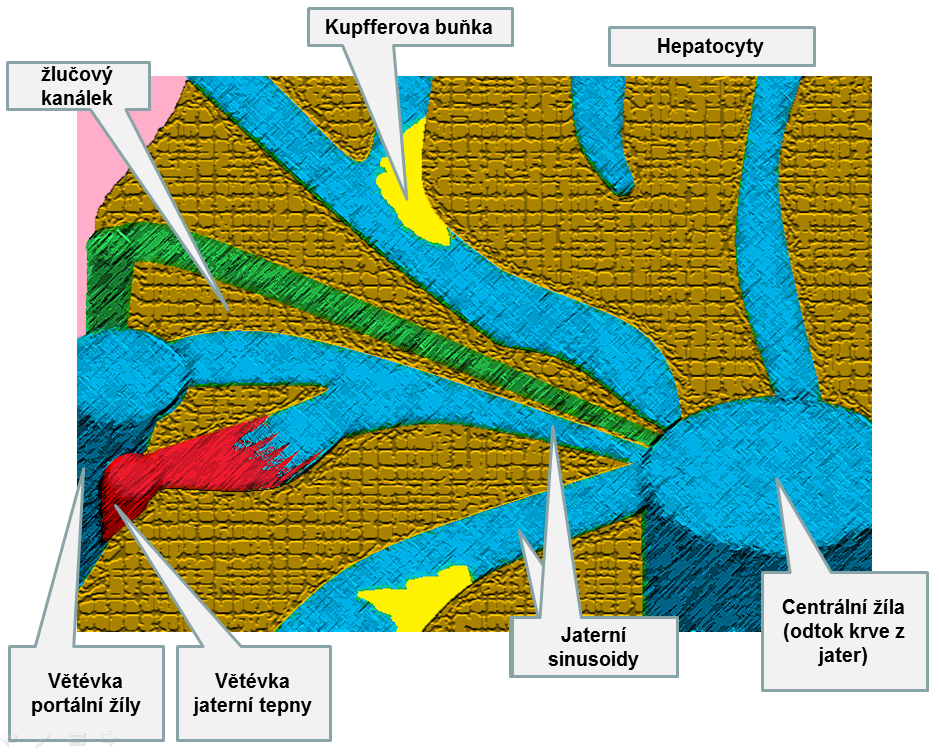
6.13 Játra a žluč
6.14 Poruchy tvorby slin
- cíleně po navození léky (viz výše), např. před chirurgickými zákroky, kdy je vhodné slinění potlačit
- při podráždění sliznice zánětem (např. anginou)
- přirozeně vlivem potravy (včetně reflexu) a jejího složení (např. velmi kořeněná potrava)
- nadměrnou nervovou stimulací (během nevolnosti, před zvracením – nadměrný vliv parasympatiku)
6.15 Poruchy polykání (dysfagie)
6.16 Gastroezofageální reflux (GER)
6.17 Poruchy žaludeční motility a sekrece
6.18 Peptický vřed
6.19 Nevolnost a zvracení
6.20 Malabsorpční syndrom
6.21 Průjem a zácpa
6.22 Ileus
6.23 Nedostatečnost slinivky břišní (pankreatická insfucience)
7 Fyziologie a patofyziologie jater
7.3 Testovací otázky
7.1 Fyziologie jater
7.1.1 Stavba jater z funkčního pohledu
7.1.2 Cévní zásobení jater
7.1.3 Základní funkce jater
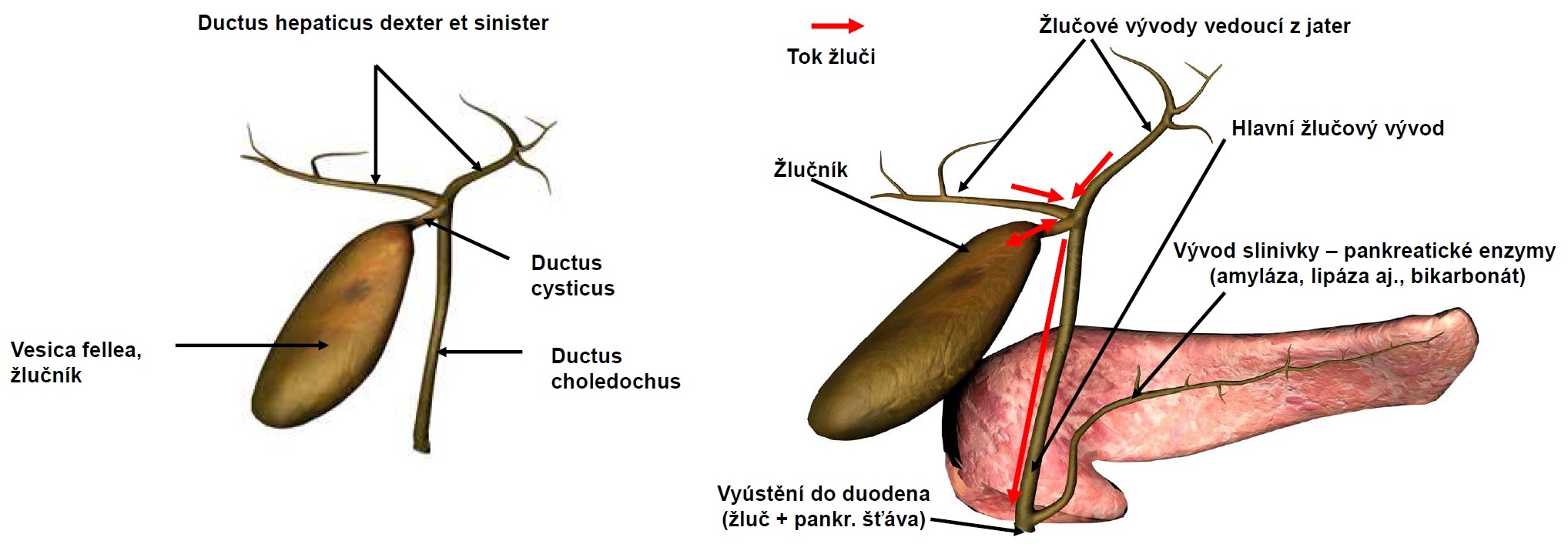
7.1.4 Fyziologie žlučových cest
7.2 Patofyziologie jater
7.2.1 Hlavní onemocnění a poškození jater
Typ |
Virus |
Přenos |
Chronicita |
Očkování |
A |
HAV |
Fekálně-orální |
Ne |
Ano |
B |
HBV |
Krev, placenta |
Ano |
Ano |
C |
HCV |
Krev, placenta |
Často |
Ne |
7.2.2 Portální hypertenze
7.2.3 Jaterní selhání
7.2.4 Ikterus
7.2.5 Cholestáza
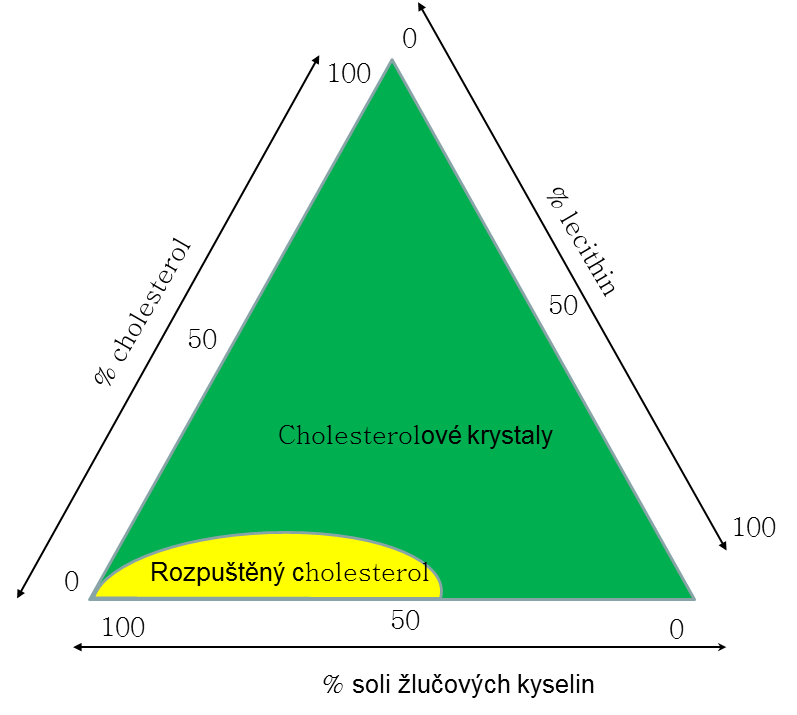
7.2.6 Žlučové kaménky
8 Fyziologie a patofyziologie metabolismu
8.5 Testovací otázky
8.1 Přehled metabolismu
8.1.1 Anabolismus
8.1.2 Katabolismus
8.1.3 Energetický metabolismus
8.1.4 Katabolické stavy a kachexie
Důsledky proteinového a energetického deficitu se prakticky dotýkají všech orgánů a tkání. Vzniká:
- úbytek tělesné hmotnosti
- zhoršení funkce myokardu, snižuje se srdeční výdej (vázne přísun okysličené krve k tkáním)
- zhoršení funkce dýchacích svalů (to je závažné, protože svaly zabezpečují ventilaci a dodávku kyslíku do plic, tedy i dále do tkání)
- zhoršení funkce žaludku, závažné změny tenkého střeva, porucha exokrinní funkce pankreatu
- změněná sekrece hormonů
- snižuje se tvorba bílkovin v játrech, klesá onkotický tlak plazmy, čímž může dojít k vzniku otoků
- snížení celkové odolnosti
- zhoršení hojení ran
8.1.5 Obezita
BMI = tělesná hmotnost v kg / druhá mocnina výšky (m)
Normální rozmezí hodnot pro BMI je 20-25, hodnota nad 25 se označuje nadváha, nad 30 pak obezita. U množství tělesného tuku je u mužů normální hodnota do 15–20 % a u žen do 25 %).
Obezita je vždy projevem dlouhodobě pozitivní energetické bilance, tj. vyššího příjmu energie než jejího výdeje. Z hlediska příčin se dělí na primární a sekundární.
Primární obezita je způsobena nadměrným příjmem potravy při nízkém výdeji, aniž je přítomna zřetelná chorobná porucha. Uplatňují se vlivy dědičné i získané (způsob stravování v raném dětství, v rodině), vlivy sociální (reklama, fast-foody, ekonomicko-sociální situace rodiny), psychické (stresy, útěk od problémů do jídla atp.). V posledních letech byl učiněn značný pokrok ve znalostech regulace příjmu potravy, ale nepodařilo se u lidí objevit jasnou příčinu, která by obezitu většiny lidí jednoduše vysvětlila. V současnosti se ve vyspělých zemích hovoří o epidemii obezity, a to už u dětí, které se jak špatně stravují, tak málo pohybují.
Obezita se dělí na tzv. obezitu s hromaděním tuku v břišní oblasti, nejen v podkoží, ale i uvnitř břicha, čili obezitu mužského typu (podle vzhledu takové osoby typu „jablko“). Lze ji zjistit měřením obvodu pasu, je typická pro metabolický (Reavenův) syndrom a je spojena s kardiovaskulárními riziky.
Obezita s hromaděním tuku kolem boků se nazývá obezitou ženského typu (podle vzhledu „hruška“). Není tak závažná s ohledem na kardiovaskulární komplikace, ale některé závažné důsledky má rovněž.
Ke komplikacím obezity mužského typu patří především:
- porucha glukózové tolerance až riziko vzniku cukrovky (diabetes mellitus 2. typu)
- častější vysoký krevní tlak (arteriální hypertenze)
- urychlení aterosklerózy
- vysoké riziko kardiovaskulárních nemocí (infarkt myokardu, cévní mozková příhoda).
- nemoci pohybového aparátu (artróza)
- kožní nemoci, opruzení, infekce
- vyšší riziko krevních sraženin a embolií (tromboembolické komplikace)
- žilní městky (varixy) na dolních končetinách
8.2 Buněčný metabolismus
8.2.1 Vznik energie
8.2.2 Zdroje energie a buněčné procesy
8.3 Metabolismus živin základních látek v lidském organismu a jeho poruchy
8.3.1 Bílkoviny
8.3.2 Sacharidy
8.3.3 Lipidy
8.3.4 Hem a bilirubin
8.3.5 Puriny a močová kyselina
8.3.6 Volné kyslíkové radikály a oxidativní stres
8.4 Vrozené metabolické poruchy
8.4.1 Obecné důsledky
8.4.2 Fenylketonurie
8.4.3 Albinismus
8.4.4 Tezaurózy
9 Fyziologie a patofyziologie výživy
9.7 Testovací otázky
9.1 Regulace příjmu potravy
9.2 Poruchy příjmu potravy
9.3 Složení potravy a její energetická hodnota
Energie (kJ) |
Bílkoviny (g) | |
děti |
9000 |
55 (do 5 let) -75 (nad 5 let) |
muži |
11000-12000 |
85 (do 50 let), 70 později** |
Ženy |
7500-9500 |
75 (55)** |
Těhotné |
11000 |
105 |
kojící |
12000 |
115 |
kJ/g |
Denní příjem |
% energetického příjmu | |
Proteiny |
17,2 |
0,8-1,5 (2,5) g/kg |
15-20 |
Sacharidy |
17,2 |
Minim. 100g |
20-30 |
Tuky |
38,9 |
50-60 |
9.4 Tělesná hmotnost a její hodnocení
9.5 Hlavní živiny
9.6 Zásady racionální výživy, dietologie, nutriční poradenství
10 Fyziologie a patofyziologie výměny tepla a kůže
10.4 Testovací otázky
10.1 Fyziologie termoregulace
10.1.1 Zdroje a produkce tepla v organismu
10.1.2 Výdej tepla
10.1.3 Tělesná teplota a její fyziologické kolísání
10.1.4 Regulace tělesné teploty
10.2 Patofyziologické aspekty termoregulace
10.2.1 Působení nadměrného tepla
10.2.2 Horečka
10.2.3 Působení nadměrného chladu
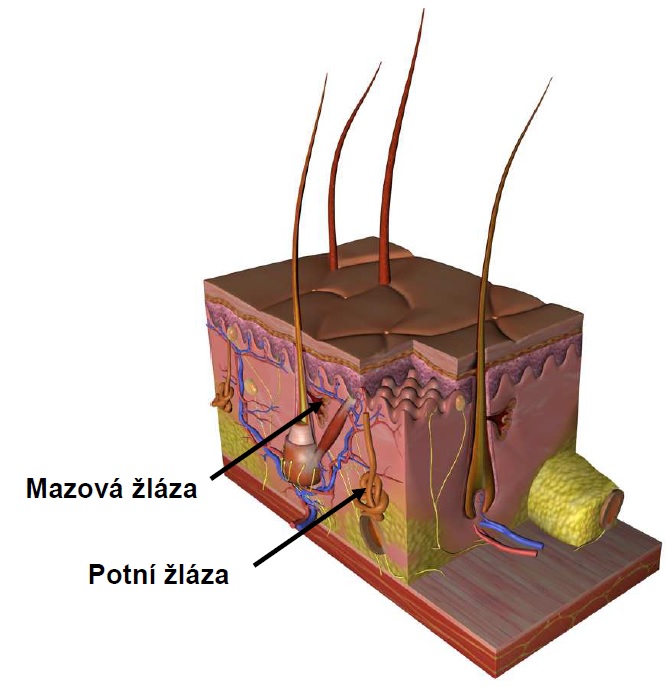
10.3 Fyziologie a patofyziologie kůže
10.3.1 Fyziologický význam kůže
10.3.2 Patofyziologické aspekty nemocí kůže
10.3.3 Vliv UV záření
11 Fyziologie a patofyziologie ledvin a vylučování
11.6 Testovací otázky
11.1 Tvorba moči
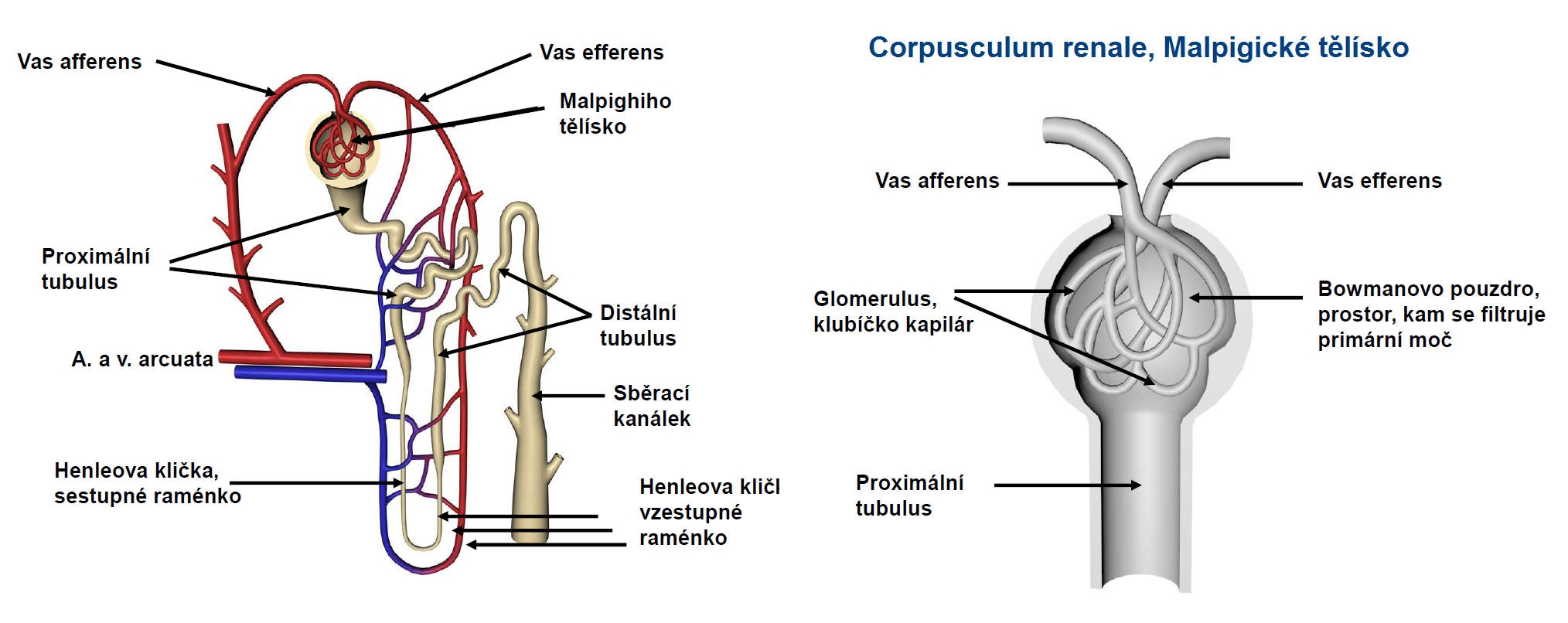
11.1.1 Princip a funkční stavba ledvin
11.1.2 Glomerulus a glomerulární filtrace (GF)
11.1.3 Tubulární část nefronu
11.2 Další funkce ledvin
11.3 Bilance látek vylučovaných močí
11.4 Složení finální moči a jeho poruchy
11.4.1 Složení moči a její vyšetření
11.4.2 Hlavní poruchy složení moči a jejich patofyziologie
11.5 Patofyziologie ledvin
11.5.1 Patofyziologie glomerulů
11.5.2 Patofyziologie tubulů
11.5.3 Akutní selhání ledvin (ASL)
11.5.4 Chronické selhání ledvin a urémie
12 Fyziologie a patofyziologie vnitřního prostředí
12.5 Testovací otázky
12.1 Úvod
12.2 Hydratace organismu a její poruchy
12.2.1 Osmolarita
12.2.2 Regulace objemu tekutin v organismu
12.2.3 Poruchy objemu tělesných tekutin a osmolarity
12.2.4 Příčiny a důsledky poruch objemu tekutin a změn osmolarity
Poruchy objemu se projevují zejm. změnami v oběhovém systému. Hypovolémie snižuje množství obíhající krve, snižuje se minutový srdeční výdej, zásobení orgánů krví a kyslíkem, je únavnost, může dojít ke kolapsům, ztrátě vědomí až smrti. Příčinou je např. krvácení, zvracení, průjmy, velké pocení, horečka a nedostatečný přísun tekutin.
12.3 Fyziologie iontového složení tekutin a jejich hlavní poruchy
Kationty (s kladným nábojem): sodík (Na+), draslík (K+), vápník (Ca++), hořčík (Mg++).
Hlavní anionty (se záporným nábojem) jsou: chloridy (Cl-), bikarbonáty (HCO3-), bílkoviny.
Iontové složení je samozřejmě elektroneutrální.
Hlavními kationty nitrobuněčnými je draslík, mimobuněčným pak sodík.
12.3.1 Sodík
12.3.2 Draslík
12.3.3 Chloridy
12.3.4 Vápník
12.4 Acidobazická rovnováha
12.4.1 pH
12.4.2 Pufry
12.4.3 Respirační a metabolická složka acidobazické rovnováhy
12.4.4 Hlavní poruchy ABR
Z výše uvedeného vyplývá, že v organismu může nastat:
Příčinou může být složka metabolická či respirační, čili mohou být 4 možnosti:
13 Fyziologie a patofyziologie žláz s vnitřní sekrecí
13.1 Základní pojmy a principy
13.1.1 Typy sekrece, žlázy v lidském organismu a jejich produkty
13.1.2 Hormony
13.1.3 Hormonům podobné látky
13.1.4 Regulace hormonální sekrece
13.2 Hypotalamus-hypofýza
13.2.1 Hypothalamus
1. antidiuretický hormon (ADH) nazývaný též vazopresin
Zvyšuje krevní tlak, protože vede k zúžení cév (proto vazopresin). Zároveň má antidiuretické účinky (snižuje množství vyloučené moči), a to účinkem na sběrací kanálky ledvin – činí je propustnými pro vodu, která se tak v této části ledvinové dřeně vstřebává zpět a moč se zahušťuje. Účinek je dán zvýšením množství molekul akvaporinu v buňkách sběracích kanálků. Stimulem pro produkci ADH je zejména vzestup osmolarity krve registrované osmoreceptory v hypothalamu (např. při nedostatku vody, žíznění, nadbytku soli); do jisté míry se množství ADH zvyšuje i vlivem stresu, bolesti a snížením objemu krve). Naopak alkohol jeho produkci tlumí. Další informace jsou v kapitolách věnovaných ledvinám a vnitřnímu prostředí.
2. Oxytocin
Hormon ovlivňující uvolňování (ejekci) mléka při kojení (nikoliv samotnou tvorbu mléka), zvyšuje stahy dělohy (uplatňuje se i jako lék k vyvolání porodu); vylučován i při orgasmu a studují se i jeho další účinky.
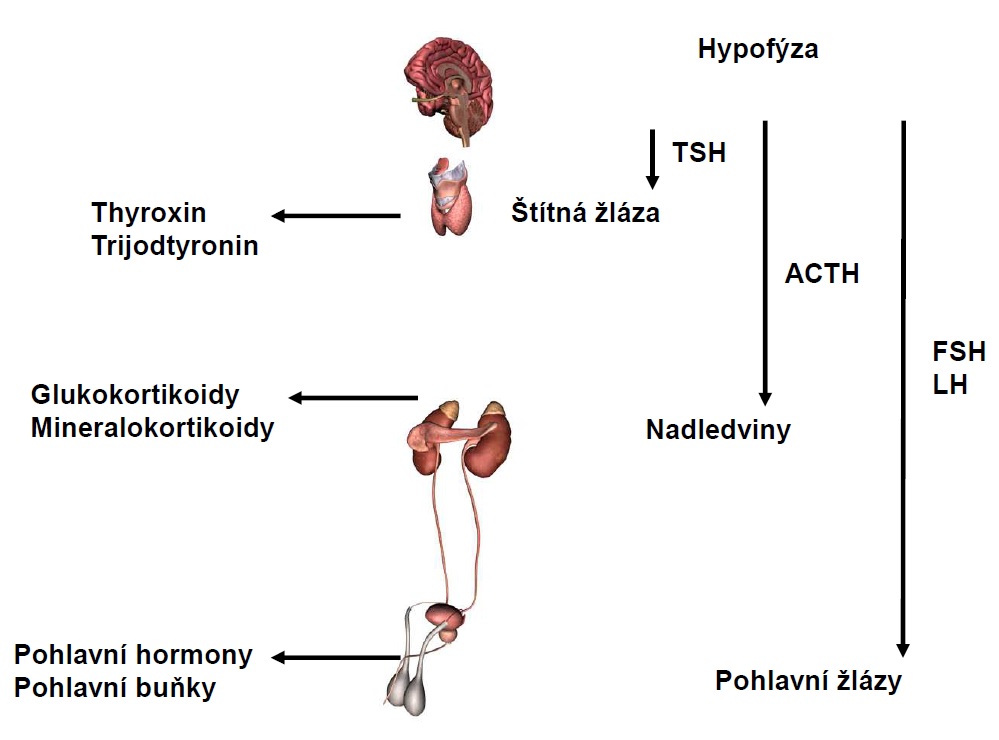
13.2.2 Hypofýza
1. ACTH (adrenokortikotropní hormon) řídí činnost kůry nadledvin, zejm. produkci glukokortikoidů
2. TSH (tyreotropní hormon) řídí činnost štítné žlázy
3. Gonadotropiny
1. růstový hormon (STH, growth hormone – GH, somatotropin). Působí na všechny orgány, ovlivňuje růst, v dospělosti pak růst akrálních částí a metabolismus. Převážně působí na zvýšení koncentrace glukózy v krvi, podporuje tvorbu bílkovin, dělení buněk. Část účinků je způsobena nepřímo, přes stimulaci tzv. IGF-1 (insulin-like growth faktoru), část přímo. Koncentrace STH v krvi fyziologicky kolísá během dne.
2. prolaktin (PRL). Je nezbytný k zahájení a udržení tvorby mléka v mléčných žlázách, tlumí produkci některých pohlavních hormonů, je významný při kojení. Z hypothalamu je tlumen dopaminem.
13.3 Žlázy regulované osou hypotalamus-hypofýza
13.3.1 Štítná žláza
13.3.2 Kůra nadledvin
13.3.3 Pohlavní žlázy a pohlavní hormony
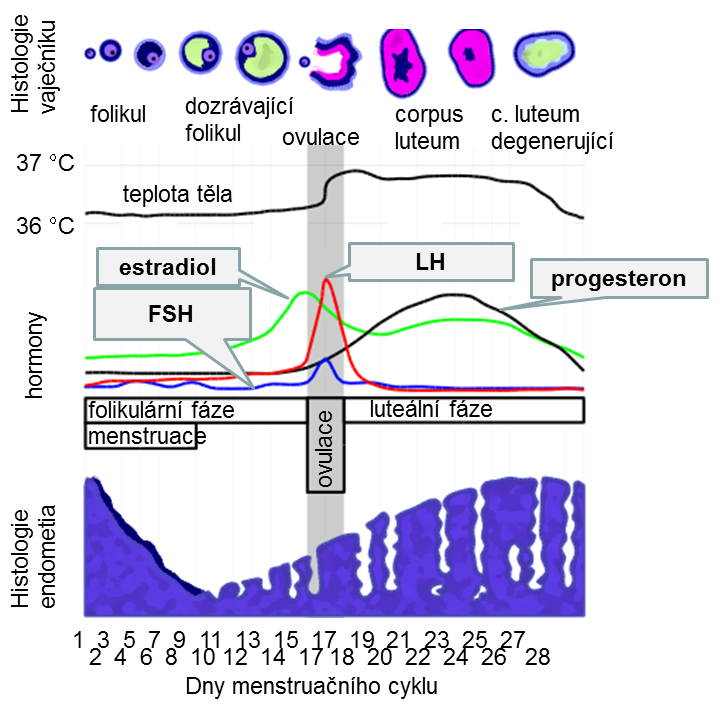
1. folikulární: vlivem FSH a částečně též LH vyzrává jeden z folikulů, mění se na velký Graafův folikul. Buňky folikulu produkují estrogeny, které pozitivní zpětnou vazbou zvyšují (!) produkci gonadtropinů z hypofýzy a jejich regulátorů z hypothalamu. Tato fáze trvá od 1. dne poslední menstruace cca 2 týdny. Ke konci jsou vysoké koncentrace estrogenů v krvi a rovněž obou gonadotropinů. Děloha je v proliferační fázi, sliznice se regeneruje po menstruaci a od cca 4. dne narůstá, přibývá v ní žlázek.
2. ovulace: uvolnění vajíčka z folikulu, koncentrace gonadotropinů jsou nejvyšší a průkaz LH v moči může být využit k stanovení ovulace (vzestup LH předchází ruptuře folikulu a je pro ovulaci zásadní)
3. luteální: po ovulaci vzniká žluté tělísko, produkující zejména progesteron, vrcholí příprava dělohy na přijetí zárodku, sliznice je v tzv. sekreční fázi, buňky jsou bohaté na zásobní látky, sliznice je nejtlustší. Tato fáze trvá cca 2 týdny od ovulace, nedojde-li k oplodnění, nastává odloučení takto připravené sliznice menstruací.
13.4 Žlázy s odlišnou regulací
13.4.1 Příštítná tělíska
13.4.2 Dřeň nadledvin
13.4.3 Endokrinní pankreas
13.5 Další látky hormonálního charakteru
13.5.1 Gastrointestinální hormony
13.5.2 Difuzní neuroendokrinní systém
13.5.3 Další hormony
13.6 Základní pojmy
V některých případech vznikají příznaky hyperfunkce v důsledku zvýšené tvorby hormonu mimo danou žlázu. To se označuje jako ektopická produkce hormonů a tímto ektopickým místem je často nádor i zcela mimo endokrinní systém (např. nádory plic mohou produkovat některé hormony).
13.7 Patofyziologie jednotlivých žláz
13.7.1 Poruchy hypothalamu
13.7.2 Poruchy hypofýzy
13.7.3 Patofyziologie štítné žlázy
13.7.4 Patofyziologie kůry nadledvin
Zvýšená funkce kůry nadledvin s nadprodukcí glukokortikoidů – hyperkortikalismus, Cushingův syndrom
13.7.5 Patofyziologie pohlavních hormonů
13.7.6 Patofyziologie příštítných tělísek
13.7.7 Patofyziologie dřeně naledvin
13.7.8 Patofyziologie endokrinního pankreatu – diabetes mellitus
13.8 Testovací otázky
14 Fyziologie a patofyziologie rozmnožování a těhotenství
14.5 Testovací otázky
14.1 Pohlaví genetické, fenotypové, sociální
14.2 Pohlavní žlázy, hormony a buňky
14.3 Reprodukční systém muže
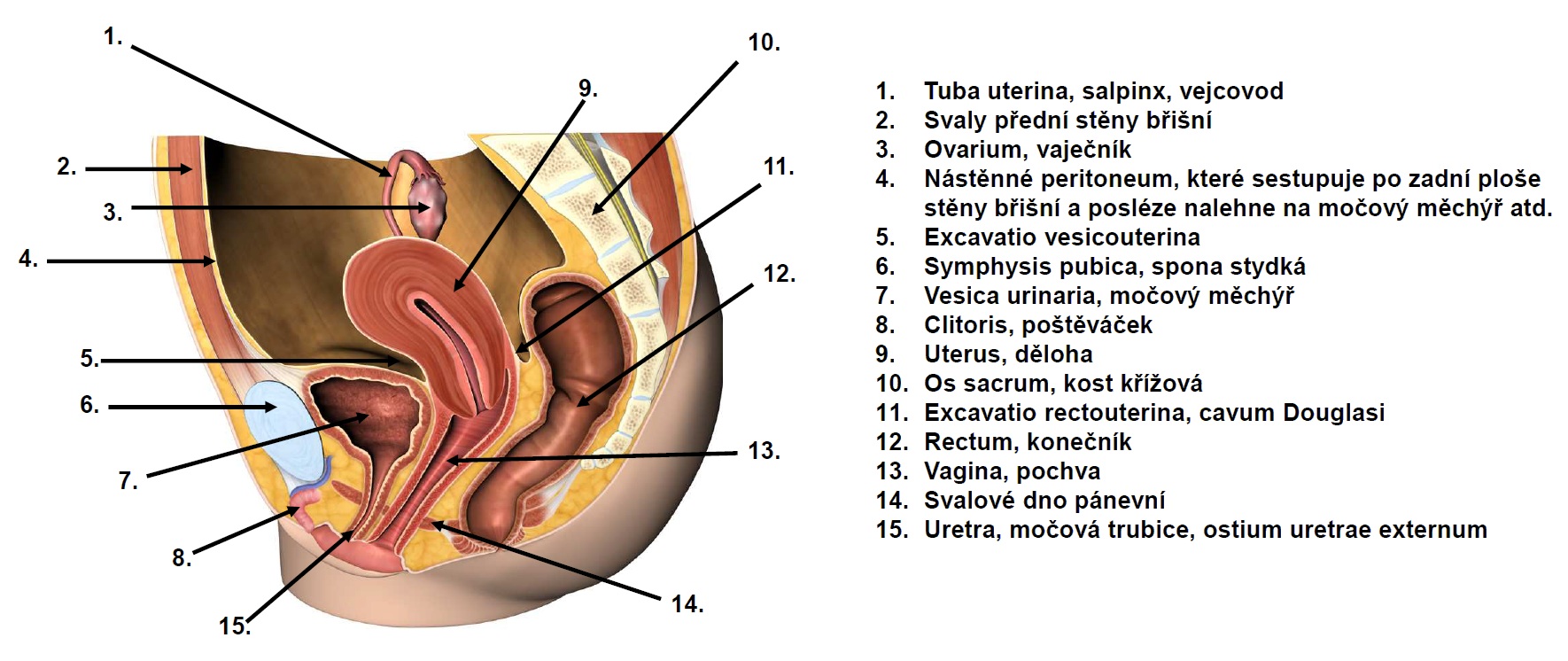
14.4 Reprodukční systém ženy
První společná buňka je zygota, následuje její dělení a uhnízdění (nidace) do děložní sliznice v sekreční fázi, dále probíhá proces embryogeneze, v němž jsou položeny základy všech orgánových systémů. Toto období je velmi zranitelné, může dojít k závažným deformacím či poruchám ve vývoji – zárodek zaniká či vznikají závažné vrozené vývojové vady. Škodlivé jsou toxické látky vč. alkoholu, drogy, některé léky a chemické látky, záření vč. rentgenového, některé infekce (toxoplasmóza, zarděnky). Neškodný je ultrazvuk. Další část je rozvoj plodu (fetus).
Těhotenství u člověka trvá přibližně 280 dnů. Během této doby dochází jak k vývoji plodu až do fáze, kdy může žít mimo dělohu (i když díky rozvoji medicíny přežívají i děti pod 1000 gramů se značnou nezralostí), tak k četným změnám v organismu matky.
15 Obecná neurofyziologie
15.12 Testovací otázky
15.1 Neurony
15.2 Synapse
15.3 Neurotransmitery
15.4 Vztahy mezi neurony
15.5 Nervová vlákna a jejich typy
15.6 Neuroglie
15.7 Reflex
15.8 Dělení nervového systému
15.9 Nervy
15.10 Vegetativní nervový systém
Sympatikus |
Parasympatikus | |
Srdce |
Zrychlení činnosti, zesílení stažlivosti, zrychlení vedení vzruchu |
Zpomalení činnosti |
Cévy |
Vazokonstrikce v útrobách (α receptory), částečně vazodilatace ve svalech, věnčitých tepnách, žilách (β2 receptory) |
Větš.vazodilatace |
Žaludek a střevo |
Uvolnění, ale kontrakce svěračů |
Zvýšení sekrece a motility |
Slinné žlázy, slinivka |
Zvýšená sekrece | |
Močový měchýř |
Relaxace vypuzovače, kontrakce svěrače |
Kontrakce vypuzovače, relaxace svěrače |
Průdušky |
Rozšíření |
Zúžení, zvýšení sekrece hlenu |
Metabolismus |
Štěpení energ. zásob |
|
Pohlavní ústrojí |
Ejakulace |
Erekce |
Oko |
Rozšíření zornice (mydriáza) |
Zúžení zornice (mióza) |
15.11 Bolest
16 Fyziologie a patofyziologie svalstva a pohybového aparátu
16.3 Testovací otázky
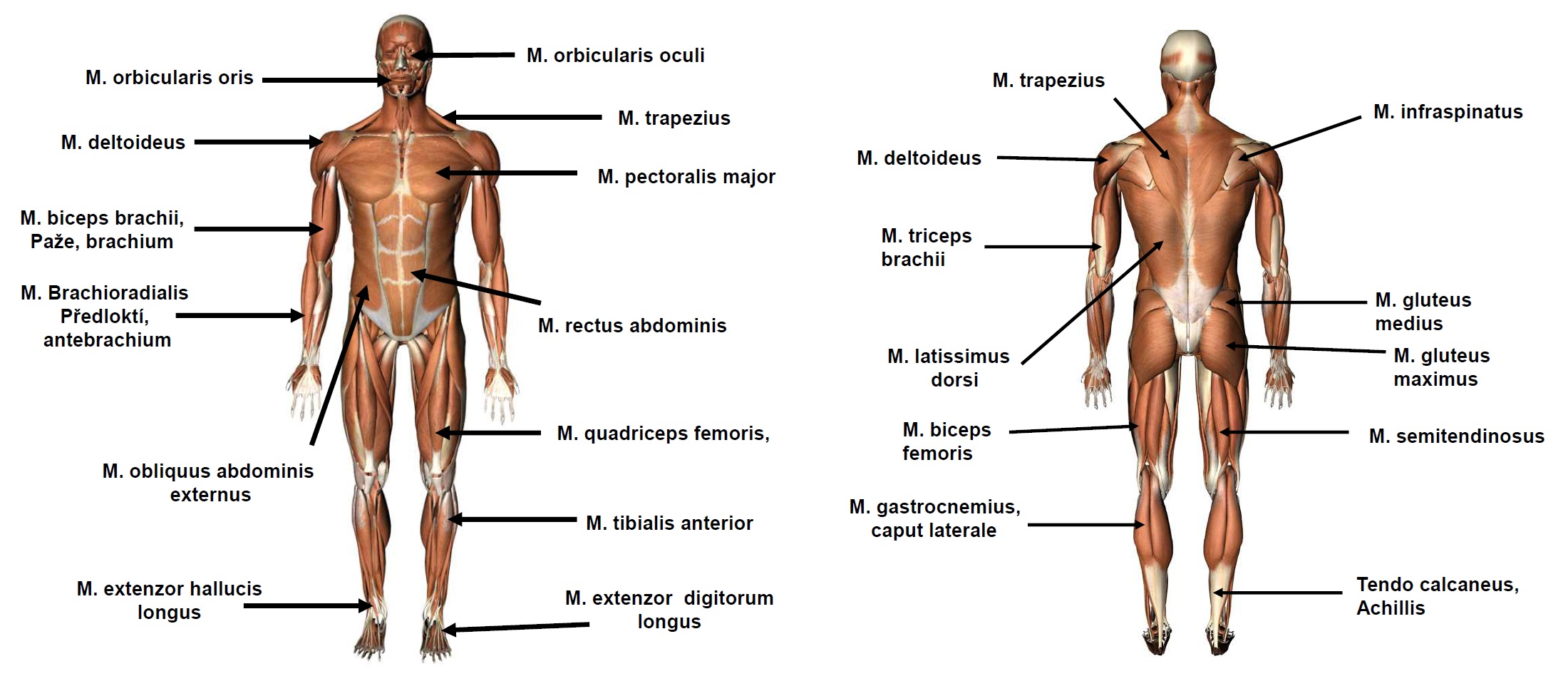
16.1 Svaly
16.1.1 Svalová kontrakce a sarkomera
16.1.2 Metabolismus a energetika svalu
16.1.3 Svalová mechanika
16.1.4 Elektrická aktivita svalu
16.1.5 Nervová regulace pohybového aparátu
16.1.6 Patofyziologie svalů
16.2 Kosti, chrupavka a klouby
16.2.1 Fyziologické principy stavby kostí
16.2.2 Funkce kostí
16.2.3 Růst a remodelace kosti
16.2.4 Patofyziologie kostí
a) pánve (deformita pánve může mít u žen závažné důsledky pro těhotenství a porod)
b) hrudníku (zhoršení funkce plic a srdce)
c) středního či vnitřního ucha (hluchota)
d) kostní dřeně (omezení krvetvorby)
16.2.5 Fyziologie a patofyziologie chrupavky
16.2.6 Fyziologie a patofyziologie kloubů
17 Fyziologie a patofyziologie CNS
17.1 Základy funkční stavby CNS
17.2 Motorické funkce – hybnost
17.3 Senzorické (aferentní) funkce
17.4 Bdění a spánek
17.5 Integrační a vyšší funkce CNS
18 Fyziologie práce
18.2 Testovací otázky
18.1 Reakce organismu na fyzickou zátěž
19 Vliv životního prostředí na fyziologické funkce
19.1 Testovací otázky