Osetrovatelska_pece_v_chirurgickych_oborech
20.1 Osteomyelitida
20.1 Osteomyelitida
Klasifikace
Osteomyelitidou nazýváme bakteriální zánět postihující kost. Dělíme ji dle průběhu, mechanizmu vzniku a původce.
Podle mechanizmu vzniku je možné odlišit osteomyelitidu hematogenní a exogenní. Hematogenní osteomyelitidu, u které je infekce do kosti zanesena krevní cestou, nalézáme nejčastěji v dlouhých kostech u dětí. Exogenní typ může vzniknout na podkladě úrazu a jeho operační léčby, přenosem infekce
z přilehlé tkáně nebo může být zanesena iatrogenně. Zvláštní forma exogenní osteomyelitidy vzniká při poruchách prokrvení jako je např. diabetická gangréna.
Osteomyelitidu můžeme rozdělit podle průběhu onemocnění na akutní a chronickou (ta se ještě dělí na aktivní a inaktivní). Akutní osteomyelitida může přejít v chronickou formu při neadekvátní terapii.
Akutní hematogenní osteomyelitida
Etiologie
Nejčastěji se vyskytuje v oblasti distálního femuru, proximální tibie a proximálního femuru v dětství. V dospělosti je vzácná a je pak nejčastěji lokalizována v obratlových tělech. Typickým původcem je Staphylococcus aureus, u novorozenců Streptococcus skupiny B a Gramm negativní bakterie. U dětí mezi 1. a 4. rokem pak Hemofilus influenzae. U novorozenců a kojenců proniká infekce z kosti do kloubu, který těžce poškozuje. Nejčastěji se akutní hematogenní osteomyelitida vyskytuje mezi 1. a 16. rokem. V té době jsou kapiláry na metafyzární straně růstové ploténky posledním větvením a. nutricia. Tyto kapiláry se prudce otáčí zpět a dosahují žilních sinusoid. V těchto místech, kde dochází ke zpomalení toku krve, je ideální situace pro zachycení bakterií a rozvoj infekce. Postupně dochází k překrvení, otoku a trombózám větví a. nutricia. Dochází tím k nekrózám a resorbci kosti. Hnisavý sekret v kosti expanduje, tlačí se skrze metafyzární kortikalis do subperiostálního prostoru, nadzvedává periost a tvoří subperiostální absces. Kortikalis poté ztrácí jak endostální tak periostální cévní zásobení a dochází k její nekróze. Tuto nekrotickou část kosti nazýváme sekvestr. Periost, který je obklopen měkkými tkáněmi přežívá a formuje obal z novotvořené kosti (nazývaný involucrum) v místě infekce.
Klinický obraz
Při rozvoji akutní hematogenní osteomyelitidy většinou dochází k prudkému zhoršení stavu pacienta, kdy se z plného zdraví objevuje vysoká teplota po předcházející třesavce. Je přítomná výrazná palpační bolestivost snad kostí (ne nad kloubem), otok, zarudnutí a zvýšená kožní teplota. Celková reakce organizmu může být velmi výrazná a ústit až do septického šoku.
Diagnostika
V krevním obraze nalézáme výraznou leukocytózu. Sedimentace erytrocytů je též vysoká. Hemokultura je pozitivní, ale pouze v polovině případů.
RTG v časném stadiu onemocnění není velkým přínosem. Prvními změnami je otok měkkých tkání. Teprve po 1-2 týdnech symptomů nalézáme osteolytické změny. Později pak zachytíme novotvořenou kost v okolí abscesu, osteopenii a také nekrotickou, sklerotickou kost nazývanou sekvestr.
Punkce subperiostálního abscesu a kultivace punktátu je důležitou diagnostickou metodou.
Terapie
Základem léčebného postupu jsou zpočátku naslepo intravenózně podávaná širokospektrá antibiotika, která po identifikaci bakteriálního agens zaměníme podle citlivosti. Nezbytná je jejich odpovídající dávka a dostatečná doba podávání. Intravenózně je podáváme přibližně 2 týdny a dále 4 týdny perorálně podle stavu pacienta. Je-li přítomen absces či sekvestr, je nezbytná chirurgická intervence. Při revizi provádíme rozsáhlé debridement devitalizovaných tkání, abychom snížili riziko chronické osteomyelitidy.
Exogenní osteomyelitida
Etilogie
Exogenní osteomyelitida se liší od hematogenní mechanizmem inokulace bakteriálního původce. K jeho zanesení dochází přímou kontaminací nebo z přilehlého ložiska infekce. Nejčastěji vzniká jako komplikace otevřených zlomenin či chirurgického výkonu. Původci jsou nejen Staphylococcus aureus a Staphylococcus epidermidis, ale též Gramm negativní organizmy či polymikrobiální infekce.
Klinický obraz
Infekce se po operačním zákroku obvykle manifestuje mezi 3. a 7. pooperačním dnem. Lokálně nalézáme napětí tkání, progredující bolest, fluktuaci, zarudnutí, otok a sekreci. Někdy je stav dramatický a dochází k dehiscenci v ráně. Přítomna bývá horečka, třesavka schvácenost a zduření regionálních mízních uzlin. Jindy, v případě méně virulentních kmenů, je rozvoj pozvolný s lehkým zarudnutím a mírnou sekrecí.
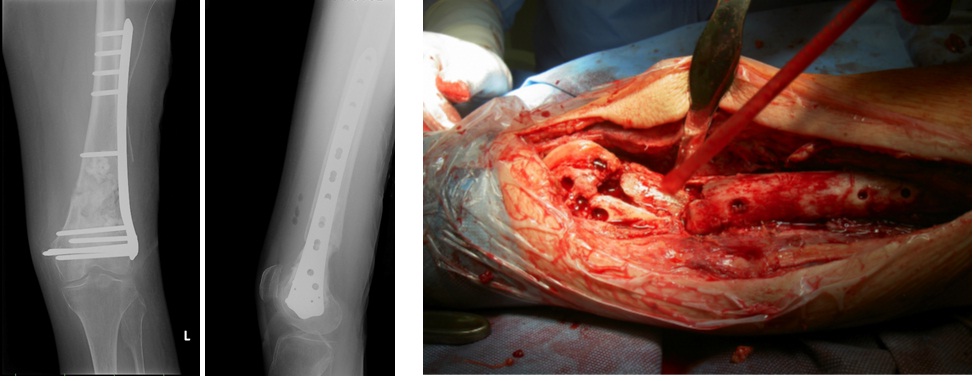
Obr. 1 a, b: RTG snímek exogenní pooperační osteomyelitidy distálního femuru s úhlově stabilní dlahou a 1c: peroperační snímek s patrným sequestrem na přední ploše stehenní kosti
Diagnostika
Sedimentace erytrocytů je často zvýšena stejně jako hodnoty CRP. Přítomna bývá leukocytóza s posunem doleva. Na RTG musíme odlišit následky úrazu či operace. Stěr infekčního materiálu a jeho kultivace je základem verifikace infekce. Odběry na kultivaci je nutno realizovat před zahájením antibiotické terapie, neboť jinak mohou být výsledky falešně negativní.
Terapie
Základem léčby jsou samozřejmě antibiotika, která však jsou bez chirurgické léčby málokdy úspěšná. Jsou-li v oblasti rány přítomny lokální známky zánětu, uvolníme několik stehů. Stále platí stará zásada „Ubi pus ibi evacua“. Došlo-li k rozvoji infekce až po zhojení rány, provádíme incizi. Základem léčby je provedení revize, radikální debridement, výplach infikovaného hematomu, užití tlakové pulzní laváže či zavedení průplachové drenáže.
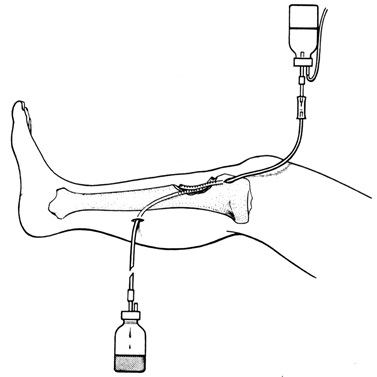
Účelem průplachové laváže je dopravovat antibiotika do místa infektu a odstraňovat z rány drobné nekrotické částice, sekret, hnis a zbytky hematomu. Zavádíme silnostěnné drény do místa zánětu. Na přívodný drén připojujeme infuzi Ringerova roztoku s antibiotikem (Neomycin, Tobramycin ev. antibiotikum dle citlivosti). Na odsavný drén napojujeme klasickou Redonovu podtlakovou odsavnou láhev. V pooperační péči je důležité pečlivě sledovat bilanci výplachové drenáže a zajistit, aby nedocházelo k retenci lavážního roztoku.
Osteosyntetický materiál je vhodné odstranit. V případě nezhojených zlomenin je třeba zvážit, zda je možno stabilitu zlomeniny zajistit jiným způsobem (zevní fixatér, extenze, sádrová fixace), či ponecháme osteosyntézu v místě infektu do zhojení zlomeniny. Stabilita zlomeniny je nezbytná pro zhojení zlomeniny. V případě, že neužijeme průplachovou laváž, můžeme do místa infekce aplikovat lokální nosiče antibiotik nejčastěji kolagenní houbu či kalcium sulfát s gentamycinem.
Obr. 2: Schéma průplachové laváže
Chronická osteomyelitida
Etiologie
Chronická osteomyelitida vzniká druhotně z akutní hematogenní či exogenní osteomyelitidy. Výjimečnými stavy jsou primárně chronické osteomyelitidy, kde se chronická infekce rozvíjí bez anamnézy akutní infekce v minulosti. Typickým původci jsou Staphylococcus aureus, Staphylococcus epidermidis a Pseudomonas aeruginoza.
Klinický obraz
Chronická osteomyelitida může mít trojí průběh: a) ataka zánětu je zaléčena, ale recidivuje bez vzniku píštělí, b) zánět zůstává v klidu, ale přetrvává píštěl, c) ataky zánětu s přetrvávající píštělí.
Podle anatomické lokalizace zánětu chronickou osteomyelitidu dělíme na formu dřeňovou, povrchovou, lokalizovanou a difúzní.
U dřeňové osteomyelitidy je primární ložisko uloženo endostálně, kdy nalézáme chronické granulace a sekvestrovanou trámčinu v dřeňovém kanálu.
Povrchová osteomyelitida se rozvíjí na zevním povrchu kosti. Predisponujícím faktorem bývá špatný stav měkkých tkání po předchozích operacích nebo cévní onemocnění.
Pro lokalizovanou osteomyelitidu je typický kortikální sekvestr. Tato forma často vzniká jako následek traumatu. Někdy se kombinuje s dvěma předchozími typy.
Při difúzní formě proniká zánět nejen celou kostí, ale šíří se i do okolních měkkých tkání.
U primární chronické osteomyelitidy chybí sekvestrace.
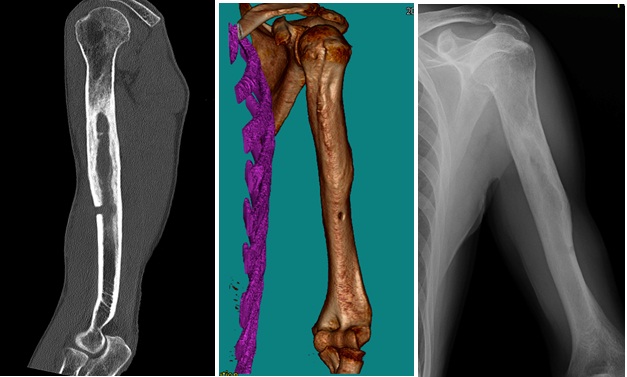
Obr. 3: CT, CT 3D a RTG snímek chronické osteomyelitidy humeru s patrnou píštělí
Diagnostika
V anamnéze pečlivě analyzujeme historii onemocnění. Sedimentace, CRP bývají zvýšeny. V RTG obrazu nalézáme typicky sekvestr - sklerotický fragment mrtvé kosti. Rentgenovou diagnostiku ztěžují též změny po předchozích operacích a úrazech. Samozřejmé je kultivační vyšetření stěrů.
Při předoperačním plánování musíme více než jindy pečlivě vyšetřit faktory ovlivňující výsledek léčby. Celkové jako je stav výživy, imunitní systém a metabolické funkce (zvláště poruchy metabolismu cukrů a ledvinné funkce). Z lokálních uveďme stav kožního krytu a cévního řečiště.
Terapie
Chronická osteomyelitida je primárně indikována k chirurgické terapii. Odstranění všech nekrotických tkání a to i měkkých je základem terapie. Provádíme pečlivé debridement, odstraňujeme píštěl, provádíme sekvestrotomii. Vzniklý prostor nesmíme ponechat volný, jinak by byl predisponujícím faktorem infekce. Proto jej vyplňujeme nosičem antibiotik, spongioplastikou, muskulokutánním lalokem či pouze zavádíme průplachovou drenáž. Obzvláště důležité je dostatečný debridement nekrotických tkání nejlépe za pomocí lžičky či frézky až do krvácející spodiny kosti, který zajistí dobrou vaskularizaci a umožní hojení.
Potlačení infekce antibiotiky dle citlivosti nejlépe intravenózně jako u všech infekcí pohybového aparátu. Snažíme se zvýšit imunitu nemocného.
Někdy je přes komplexní přístup s posílením imunitního sytému a celkového stavu pacienta léčba dlouhodobě neúspěšná. Poté pouze antibiotickou terapií potlačujeme klinickou manifestaci infekce. Stejně postupujeme v případech, kdy celkový stav pacienta není únosný k radikální operační terapii.