Máte zapnutý náhled celé osnovy, zpět na běžné zobrazení.
Načítání a prohlížení osnovy může být v závislosti na množství obsahu pomalejší.
Ošetřovatelská péče o nemocné v chirurgických oborech
-
10.1 Historie ošetřování chronických ran
-
10.2 Rozdělení chronických ran
-
10.3 Typy hojení ran
-
10.4 Terapeutická krytí rány
-
10.5 Další léčebné postupy
-
10.6 Role sestry při péči o chronické rány
-
10.7 Hojení ran a význam nutrice
-
10.8 Komplikace při hojení ran
-
10.9 Ošetřovatelská péče u pacienta s chronickou ranou
-
25.1 Rizikové faktory
-
25.2 Patologické formy karcinomu plic
-
25.2.1 Karcinom epidermoidní (z plochých buněk – skvamózní)
-
25.2.2 Adenokarcinom
-
25.2.3 Bronchoalveolární karcinom
-
25.2.4 Karcinom z velkých buněk (obrovskobuněčný karcinom)
-
25.2.5 Adeno-epidermoidní karcinom (adenoskvamózní)
-
25.2.6 Karcinoidy
-
25.2.7 Karcinomy z bronchiálních žlázek
-
25.2.8 Malobuněčný karcinom plic (karcinom z ovískových buněk)
-
25.2.9 Nemalobuněčný karcinom plic
-
-
25.3 Klinický obraz
-
25.4 Diagnostika
-
25.5 Rozvaha o operaci
-
25.6 Chirurgická léčba plicních nádorů
-
25.6.1 Důvody nízké operability
-
25.6.2 Indikace a kontraindikace chirurgické léčby
-
25.6.3 Onkologické kontraindikace
-
25.6.4 Somatické kontraindikace
-
25.6.5 Typy plicních operací
-
25.6.6 Rozšířené plicní výkony
-
25.6.7 Provedení lobektomie
-
25.6.8 Předoperační vyšetření
-
25.6.9 Funkční vyšetření plic
-
25.6.10 Předoperační příprava
-
25.6.11 Pooperační komplikace
-
25.6.12 Metastatické nádory plic
-
-
25.7 Transplantace plic
1 Ošetřovatelský proces u pacienta s vředovou chorobou žaludku a duodena
1.1 Testovací otázky
2 Ošetřovatelský proces u pacienta s nádorem žaludku
2.9 Testovací otázky
2.1 Epidemiologie
2.2 Etiologie
2.3 Klasifikace karcinomu žaludku a prognóza
2.4 Klinická symptomatologie
2.5 Diagnostika
2.6 Terapie karcinomu žaludku
2.7 Pooperační postresekční syndromy
2.8 Prevence
3 Ošetřovatelský proces u pacienta s karcinomem tlustého střeva
3.3 Testovací otázky
3.1 Ošetřovatelský proces u pacienta s kolorektálním karcinomem
3.1.1 Rizikové faktory kolorektálního karcinomu
3.2 Stomie
3.2.1 Komplikace kolostomie
3.2.2 Péče o stomii
4 Ošetřovatelský proces u pacienta s apendicitidou
4.1 Testovací otázky
Ošetřovatelské diagnózy:
- akutní bolest - 00132
- nedostatečné znalosti – 00126
- hypertermie - 00007
- nauzea - 00134
- narušená integrita tkáně - 00044
- nespavost - 00095
- průjem - 00013
- riziko sníženého objemu tekutin v organizmu - 00028
- riziko infekce - 00004
- riziko perioperačního poškození - 00087
- strach - 00148
- únava - 00093
- úzkost - 00146
5 Ošetřovatelský proces u pacienta s herniemi
5.1 Testovací otázky
6 Ošetřovatelský proces u pacienta s ileozním stavem
6.1 Testovací otázky
7 Ošetřovatelský proces u pacienta s onemocněním žlučníku a žlučových cest
7.6 Testovací otázky
7.1 Cholelitiáza
7.2 Zánětlivá onemocnění
7.3 Nádory žlučového systému
7.4 Diagnostika při onemocnění žlučových cest
7.5 Léčba při onemocnění žlučových cest
8 Ošetřovatelský proces u pacienta s onemocněním pankreatu
8.6 Testovací otázky
8.1 Akutní zánět slinivky břišní
8.1.1 Epidemiologie
8.1.2 Etiologie
8.1.3 Patogeneze a patofyziologie
8.1.4 Klasifikace akutní pankreatitidy
8.1.5 Diagnóza a klinický obraz
8.2 Léčba akutní pankreatitidy
8.2.1 Konzervativní léčba
8.2.2 Chirurgická léčba
8.3 Chronická pankreatitida (CHP)
8.3.1 Klinický obraz
8.3.2 Diagnostika
8.3.3 Léčba
8.4 Karcinom pankreatu
8.4.1 Patologie
8.4.2 Klinický obraz
8.4.3 Diagnostika
8.4.4 Léčba
8.5 Léčba bolesti
9 Ošetřovatelský proces u pacienta s Crohnovou nemocí
9.5 Testovací otázky
9.1 Příčiny onemocnění
9.2 Klinický průběh
9.3 Diagnostika
9.4 Léčba
9.4.1 Konzervativní léčba
9.4.2 Chirurgická léčba
10 Ošetřovatelský proces u pacienta s chronickou ránou
10.10 Testovací otázky
10.1 Historie ošetřování chronických ran
10.2 Rozdělení chronických ran
10.3 Typy hojení ran
10.4 Terapeutická krytí rány
10.5 Další léčebné postupy
10.6 Role sestry při péči o chronické rány
10.7 Hojení ran a význam nutrice
10.8 Komplikace při hojení ran
10.9 Ošetřovatelská péče u pacienta s chronickou ranou
11 Ošetřovatelský proces u pacienta s tromboflebitidou
11.1 Testovací otázky
Tromboflebitida je zánětlivé a trombotické postižení povrchových žil. Na rozdíl od flebotrombosy (trombosy) kdy se jedná o vznik krevní sraženiny v hlubokých žilách končetiny. Vyskytuje se jak na horních i dolních končetinách.
12 Ošetřovatelský proces u pacienta s revmatoidní artritidou
12.10 Testovací otázky
12.1 Dělení revmatických onemocnění
12.2 Etiologie
12.3 Diagnostika
12.4 Zánětlivá revmatická onemocnění
12.4.1 Revmatoidní artritida
12.4.2 Systémová autoimunitní onemocněni pojiva
12.4.3 Spondylartritidy
12.5 Degenerativní kloubní onemocnění
12.6 Metabolická kostně-kloubní onemocnění
12.7 Mimokloubní revmatismus
12.8 Léčba revmatických chorob
12.9 Nejčastější ošetřovatelské diagnózy
13 Ošetřovatelský proces u pacienta s osteoartrózou
13.5 Testovací otázky
13.1 Etiologie
1. Mechanické přetížení
2. Kloubní diskongruence
3. Aseptická nekróza kloubní (u alkoholiků, nemocných pod kortikosteroidy apod.).
4. Metabolická systémová onemocnění (ochronóza, Gaucherova nemoc, krystalové artropatie - dna).
5. Chronické kloubní záněty (revmatoidní artritidy, psoriasa, hnisavá artritida). Vzniklé poškození chrupavky je u obou typů artrózy zcela ireverzibilní.
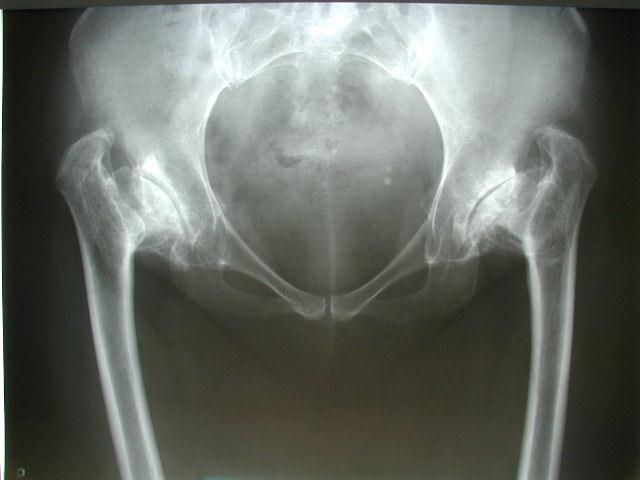
Obr. 1 : RTG snímek pánve s postdysplastickou artrózou III. stupně. Je patrné zúžení, mělké strmé acetabulum a plochá hlavice s výraznou subchondrální sklerózou
13.2 Klasifikace
13.3 Konzervativní léčba
13.4 Chirurgická léčba
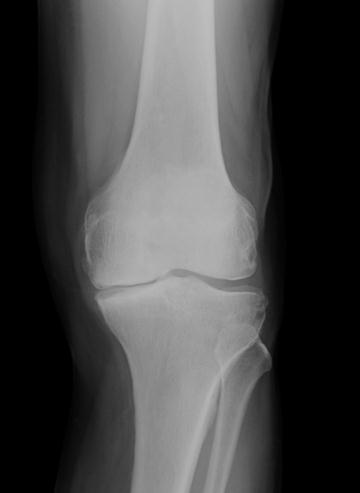
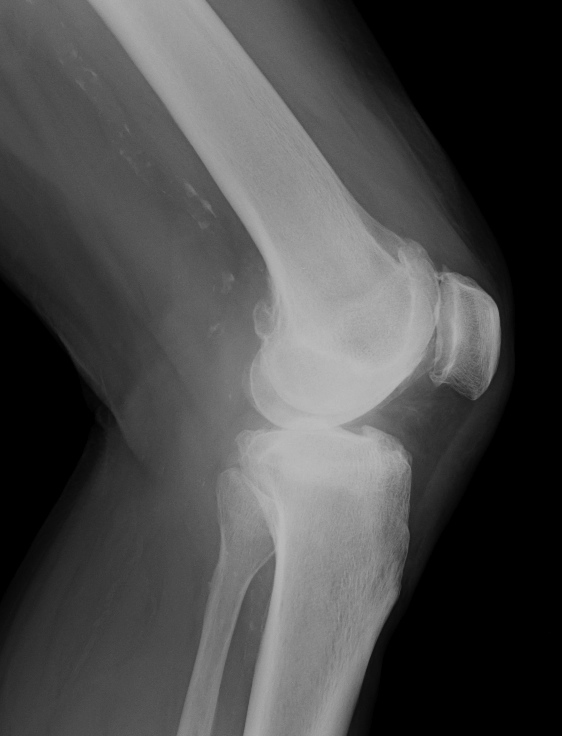
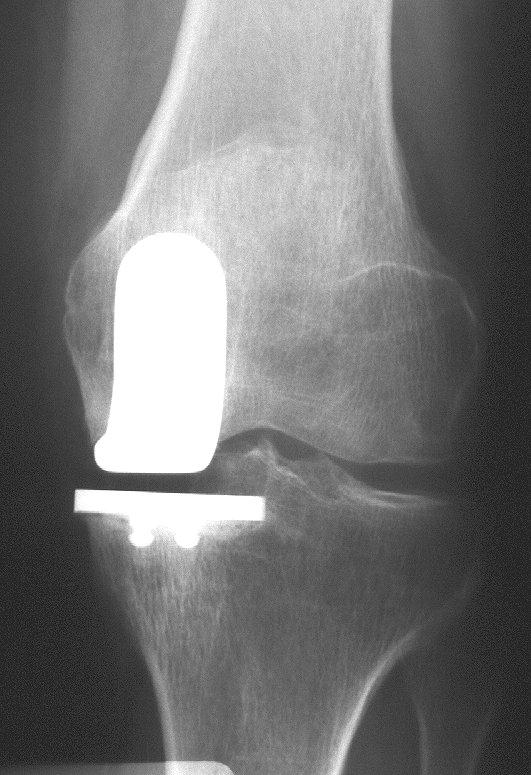
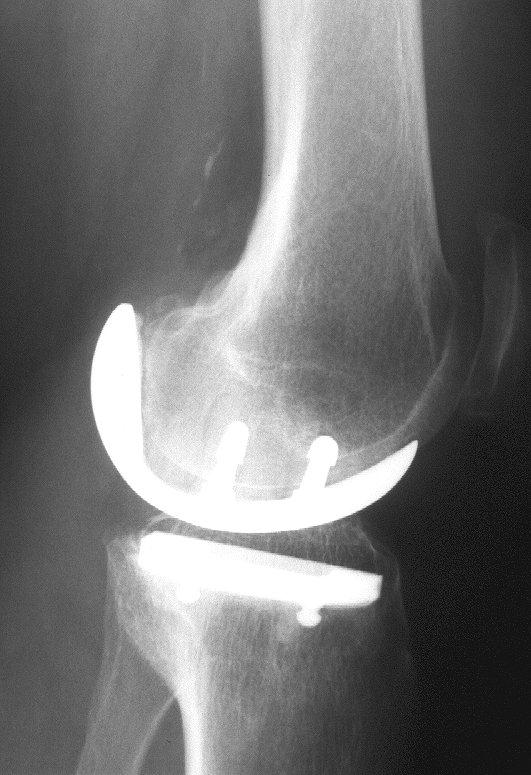
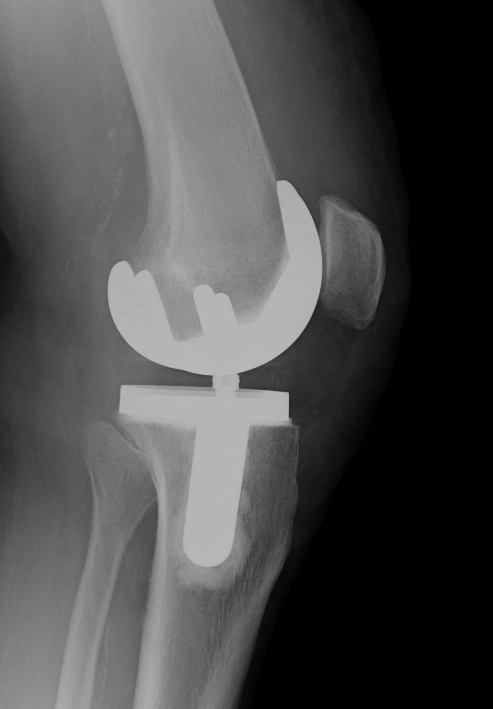
Obr. 7 a,b: RTG snímek kolenního kloubu s implantovanou hemiarhroplastikou
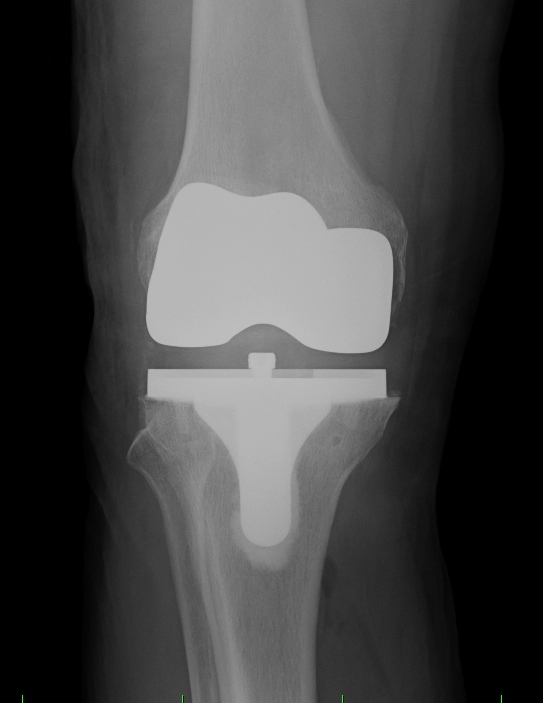
Obr. 8a,b: RTG snímek kolenního kloubu s implantovanou kondylární náhradou SVL fixovanou kostním cementem
14 Ošetřovatelský proces u pacienta po totální laryngektomii
14.7 Testovací otázky
14.1 Anatomie a funkce hrtanu
14.1.1 Anatomie hrtanu
14.1.2 Funkce hrtanu
14.2 Karcinom hrtanu
14.2.1 Výskyt a příčiny
14.2.2 Symptomy a klinický nález
14.2.3 Diagnostika
14.2.4 Léčba
14.3 Tracheostomie
14.3.1 Vliv tracheostomie na fyziologické funkce
14.3.2 Tracheostomické kanyly
14.3.3 Péče o tracheostoma a výměna tracheostomické kanyly
14.4 Náhradní hlasové mechanizmy
14.4.1 Jícnový hlas - ruktus
14.4.2 Hlasová protéza v tracheoezofageálním shuntu (píštěle)
14.4.3 Elektrolarynx
14.5 Kvalita života po totální laryngektomii
14.5.1 Adaptace na životní změnu
14.5.2 Foniatrická péče
14.5.3 Pomůcky zlepšující kvalitu života
14.5.4 Sdružení osob s podobným postižením
14.6 Nejčastější ošetřovatelské diagnózy
15 Ošetřovatelský proces u pacienta s vertebrogenním algickým syndromem
15.9 Testovací otázky
15.1 Etiologie
15.2 Diagnostika
15.3 Degenerativní onemocnění páteře
15.4 Zánětlivá onemocnění páteře
15.5 Nádorová onemocnění
15.6 Chronický algický vertebrogenní syndrom
15.7 Komplexní léčebná rehabilitace
15.8 Ošetřovatelská péče při chirurgické léčbě
16 Ošetřovatelský proces u pacienta s poraněním měkkého kolena
16.4 Testovací otázky
DUNGL P. Ortopedie. Praha: Grada, 2005. 1273s. ISBN 80-247-0550-8.
16.1 Poranění vazů
16.2 Poranění menisků
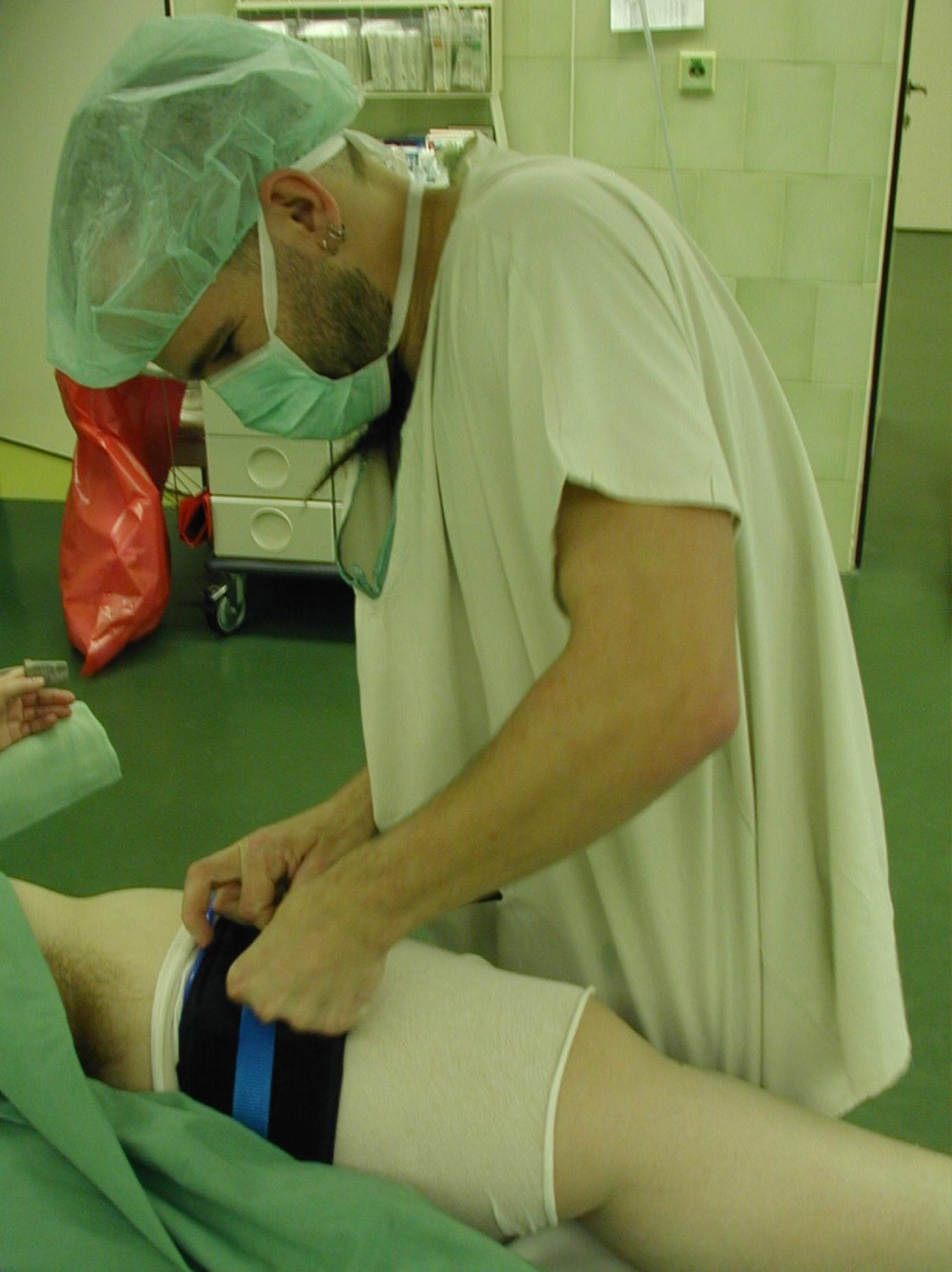
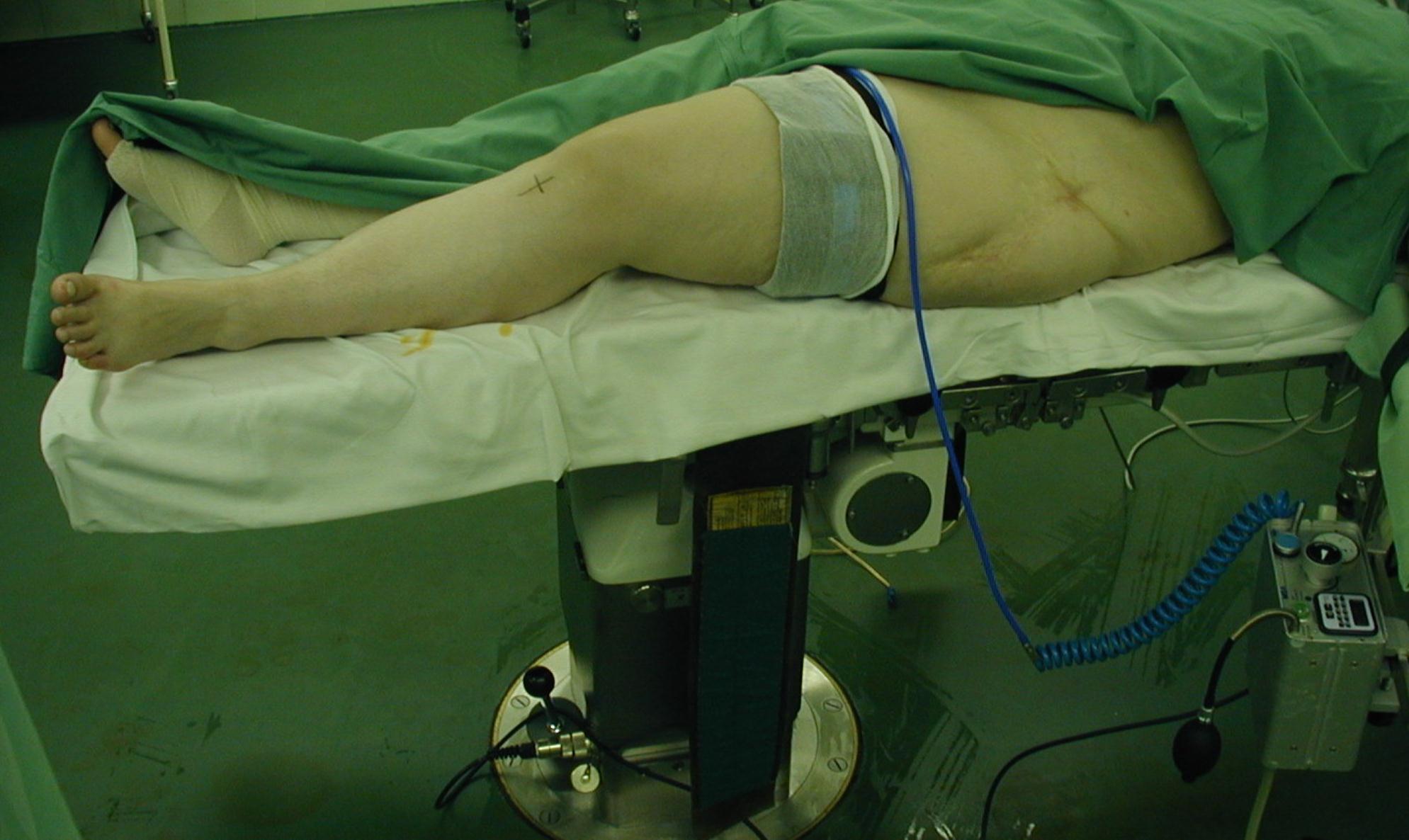
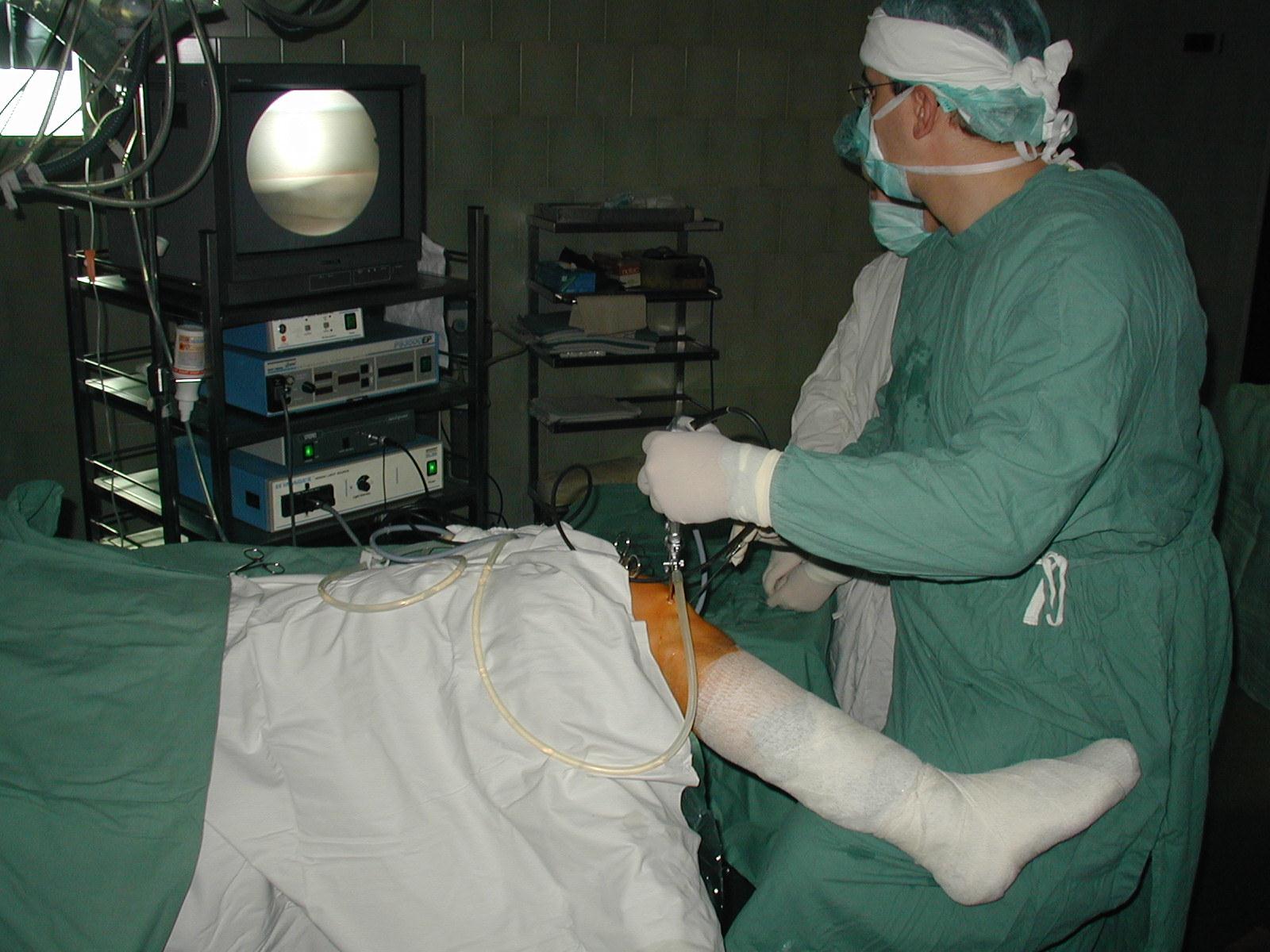
16.3 Artroskopie
17 Ošetřovatelský proces u pacienta s vrozeným vykloubením kyčelního kloubu
17.4 Testovací otázky
17.1 Etiologie
17.2 Diagnostika
17.3 Léčení
18 Ošetřovatelský proces u pacienta s frakturou horní a dolní končetiny
18.7 Testovací otázky
18.1 Dělení zlomenin
18.2 Diagnóza zlomeniny
18.3 Hojení zlomeniny
18.4 Léčba zlomeniny
Tibiální zajištěný hřeb Synthes Expert (z materiálu firmy Synthes)
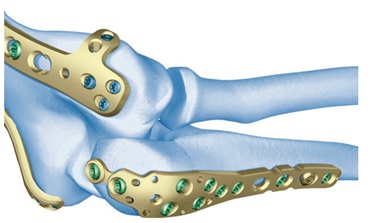
Úhlově stabilní dlaha LCP dlaha firmy Synthes na olecranon a distální humerus (z materiálu firmy Synthes)
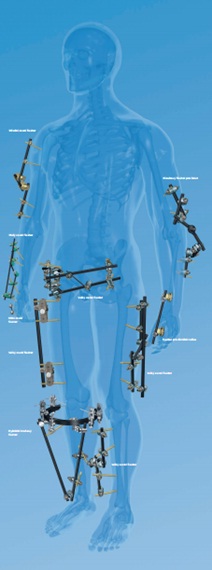
Možnosti využití zevních fixatérů (z materiálu firmy Synthes)
18.5 Horní končetina
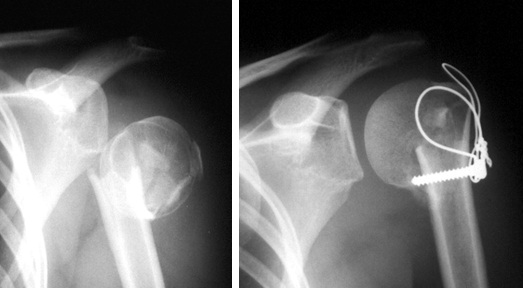
Zlomenina horního konce pažní kosti a osteosyntéza tahovou cerkláží
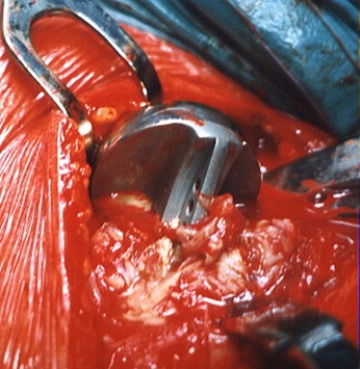
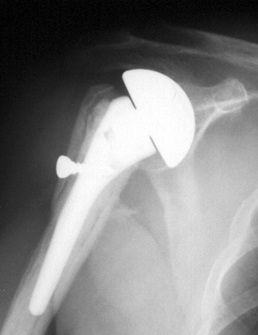
Cervikokapitální náhrada ramenního kloubu
RTG snímek cervikokapitální náhrady ramenního kloubu
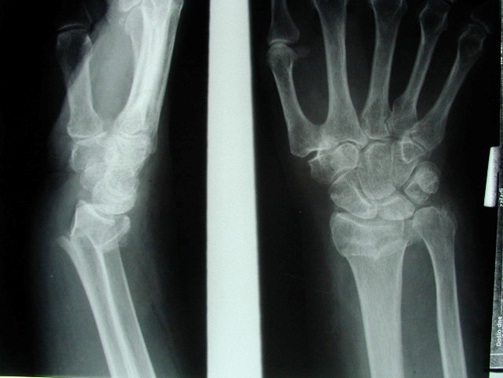
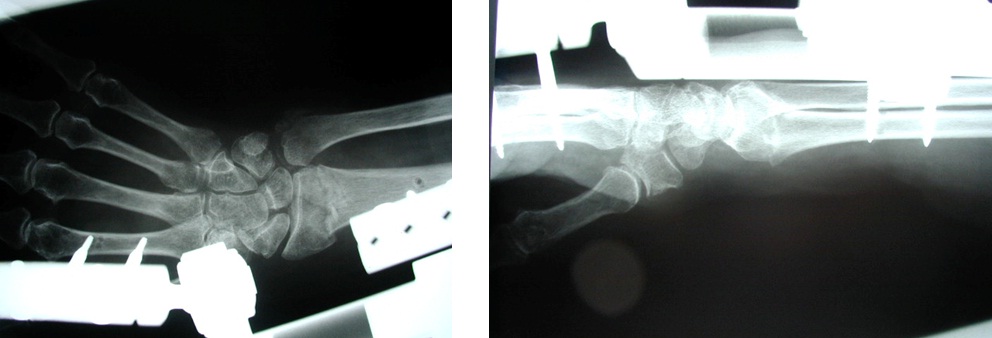
Nestabilní intraartikulární zlomenina distálního rádia Collesova typu
18.6 Dolní končetina
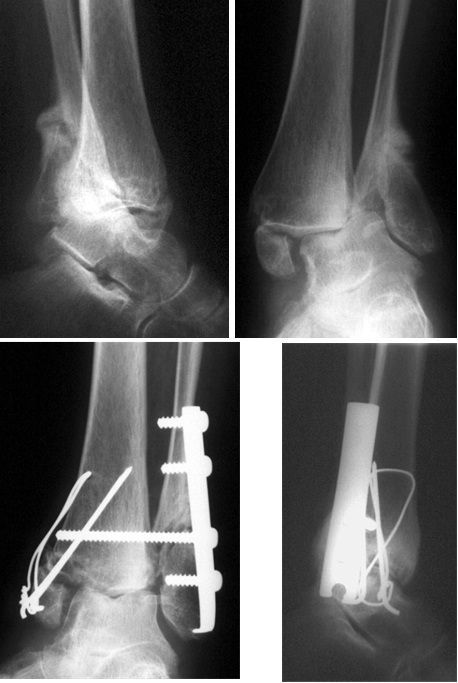
RTG snímek zlomeniny hlezna AP a bočná projekce a její řešení dlahou na fibule a tahovou cerkláží mediálního kotníku
19 Ošetřovatelský proces u pacienta po amputaci končetiny
19.8 Testovací otázky
Velkým zlomem bylo zavedení ligatury velkých cév Francouzem Ambroise Paré, které nahradilo hemostázu vařícím olejem. Tato metoda spolu s vývojem anestezie, zavedení asepse, odložené primární sutury a užití antibiotik umožnila tvarování dobře proteticky ošetřitelných pahýlů.
S dalším rozvojem válečné medicíny se nejen zlepšily techniky amputací a zmodernizovaly typy protéz. S rozvojem nových medicínských technik, zvláště rekonstrukční cévní chirurgie, za korejské a vietnamské války, se podařilo omezit nutnost indikací k amputaci. Další rozvoj ortopedické protetiky zvýšil kvalitu života pacientů.
SOSNA, A., VAVŘÍK, P., KRBEC, M., POKORNÝ, D. a kol. Základy ortopedie. Praha: Triton, 2001. 180 s. ISBN 80-7254-202-8.
19.1 Indikace k amputaci
Nejčastěji je indikována amputace u diabetické angiopatie ústící do diabetické gangrény s infekcí a dále u akutní či chronické arteriální insuficience. Vzhledem k systémovému charakteru onemocnění je třeba úzké multioborové spolupráce při přípravě pacienta k operaci. Ve spoluprácí s angiology a diabetology se taktikou „limb saving surgery“ snažíme se zachovat co nejdelší pahýl tak, aby mobilita pacienta byla zachována.
Trauma
Amputace je indikována u devastujících poranění, kde není možná rekonstrukce jednotlivých struktur a dále u komplikací jako je plynatá sněť, kterou se nedaří zvládnout antibiotiky, oxygenoterapií a chirurgickým ošetřením a u cévních poranění s gangrénou končetiny.
Tumory
Amputaci jako radikální řešení u maligních tumorů, event. jako paliativní zákrok u generalizovaných tumorů s exulcerací, nesnesitelnými bolestmi či s patologickou zlomeninou indikujeme díky moderním onkologickým metodám stále méně často. Benigní tumory vyžadují amputaci jen výjimečně (nevhodná lokalizace, velikost).
Infekce
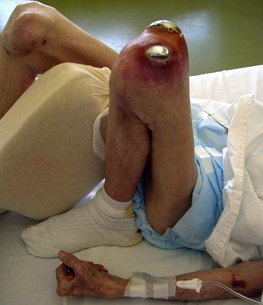
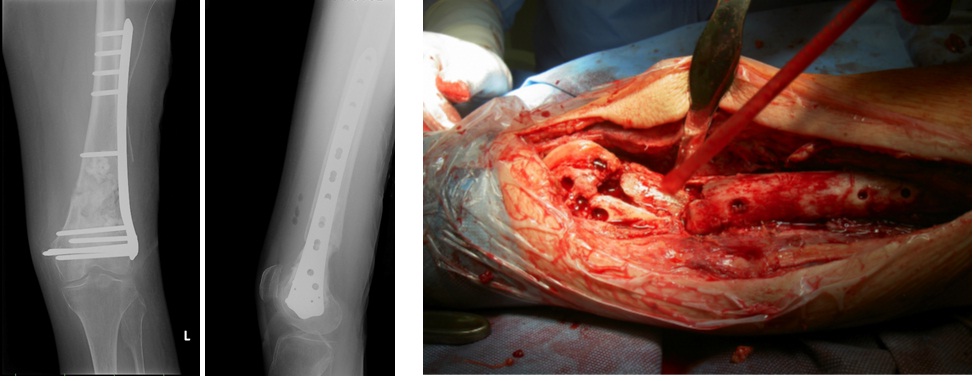
Další indikací jsou nezvládnutelné akutní infekce a chronické osteomyelitidy nezvládnutelné komplexní terapií. Hraniční indikací je i infekce náhrady kolenního kloubu.
Obr. 1: Infekce náhrady kolenního kloubu způsobená špatnou ošetřovatelskou péčí a rozvojem flekční kontraktury. Jedinou možností léčby je amputace ve stehně.
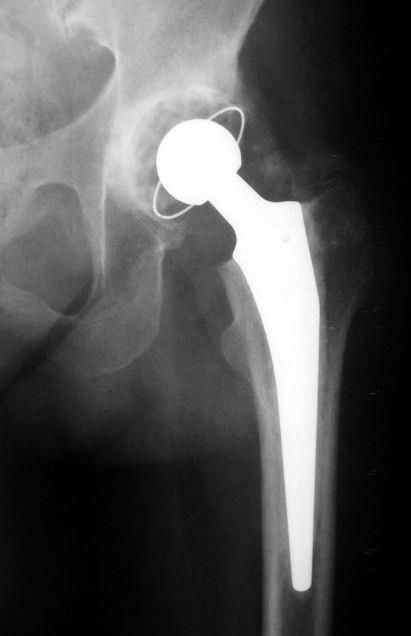
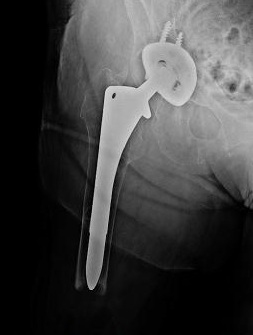
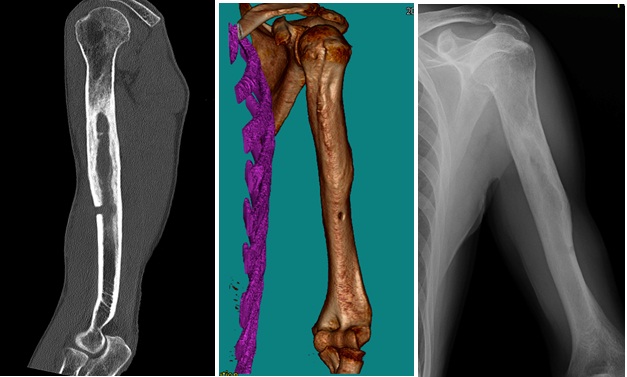
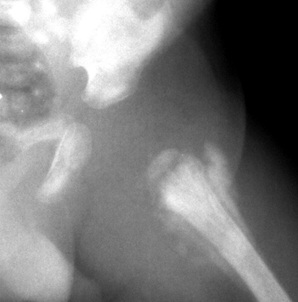
Obr. 2: RTG dokumentace kyčelního kloubu a stehenní kosti u pacientky s revmatoidní artritidou, na kterém sice dominuje náhrada kyčelního kloubu, ale po bližším zkoumání je patrné,že femorální komponenta vyplňuje amputát stehenní kosti. Indikací k amputaci ve stehně byla infekce náhrady kolenního kloubu a 10 revizních operací s defektem měkkých tkání.
Vrozené vady jsou indikovány k amputaci pouze tehdy, jestliže je malformovaná končetina afunkční a není možné její ortoticko-protetické ošetření.
Onemocnění nervové soustavy
Indikací k amputaci jsou také neuropatie ústící v trofické vředy, jež se druhotně infikují a ohrožují končetinu i život pacienta. U paraplegiků indikujeme amputaci zcela výjimečně, neboť končetiny pomáhají udržet rovnováhu na invalidním vozíku a slouží k rozložení hybnosti a tak vedou k prevenci dekubitů.
19.2 Chirurgické principy amputací
Stanovení výše amputace
Dříve byly doporučovány určité typy amputací, tak aby bylo možné zhotovení funkční protézy. Nyní s pokrokem protetické techniky se rozhodujeme dle lokálního nálezu a chirurgických možností. Amputace se provádí ve tkáni, která umožní dobré zhojení. Je-li indikací k amputaci cévní onemocnění, je třeba zmapovat prokrvení končetiny za pomoci arteriografie, dopplerova ultrazvukového vyšetření a dalších metod, jako je transkutánní stanovení hladiny P02 a radionuklidové angiografie. U tumorů záleží na typu nádoru a stupni generalizace procesu.
Vlastní výkon
Turniket užíváme vždy, je-li to možné. Operace je pak snadnější, operační pole přehlednější. Neužíváme jej však u výkonů z cévní indikace.
Dříve se svaly protínaly ve výši amputace. V současnosti se užívá tzv. myoplastická amputace. Svaly se protínají mírně distálně (10 cm) od plánované kostní amputace a protilehlé svalové skupiny se sešijí k sobě přes vrchol kostního pahýlu pod přiměřeným napětím. Tento způsob ošetření umožňuje využití svalové funkce pro pohyb, zlepšuje cirkulaci krevní, brání vzniku fantomových bolestí a optimalizuje tvar amputačního pahýlu.
Velké cévní kmeny se izolují a ošetřují podvazem (artérie a vény samostatně). Před uzavřením rány se uvolňuje turniket a pečlivě se staví krvácení jak koagulací, tak podvazy - ligaturami. Důsledná hemostáza je podmínkou dobrého hojení amputačního pahýlu. Názory na ošetření nervového pahýlu jsou nejednotné. Nejběžnější je povytáhnutí nervu z operačního pole a jeho protětí ostrým skalpelem. Ligaturu nervu stehem nedoporučujeme.
Osteotomii provádíme oscilační pilou, bez sloupávání (strippingu) periostu. Kostní prominence mají být zkoseny. Fibula se při amputaci v bérci zkracuje proti holenní kosti asi o 1 cm.
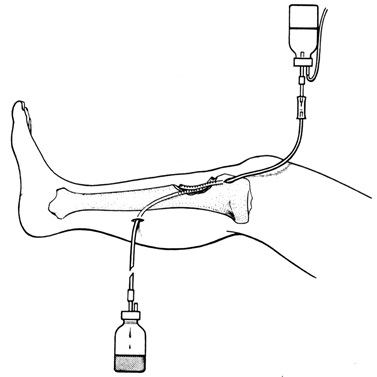
Ránu zajišťujeme Redonovou odsavnou drenáží na 48-72 hodin podle velikosti krevních ztrát. Prevence hematomu je důležitá, neboť napětí tkání vyvolané hematomem je nejen zdrojem bolestí, ale především zpomaluje hojení a je také vhodným místem pro rozvoj případné infekce.
Uzavření amputačního pahýlu kvalitním kožním krytem je nesmírně důležité a to bez ohledu na výšku amputace. Sutura musí být provedena bez napětí. Kůže na konci pahýlu má být mobilní, citlivá a dobře prokrvená.
Při skončení operace je rána kryta mastným tylem a sterilní gázou. Přes ni dáváme vatu, obinadlem tvarujeme postupně tvar pahýlu. Obvaz ukončujeme škrobovým obinadlem s dřevěno-dýhovou výztuží (furnýry) křížem přes sebe chránícími citlivý vrchol pahýlu.
Po převezení nemocného z operačního sálu je důležité správně polohovat končetinu. Pro prevenci pooperačního otoku je nutná elevace operované končetiny. Ta však nesmí být zajištěna podložením pahýlu ve flexi. Toto polohování vede k nenapravitelným flekčním kontrakturám, jež těžce poškozují pacienta. Elevaci končetiny zajistíme nastavením lůžka.
Drény odstraňujeme za 48-72 hodin dle ztrát. Stehy extrahujeme mezi 10. a 14. dnem v případě normálního hojení.
Základem dobrého fungování protézy je dobře tvarovaný pahýl. O jeho tvaru se samozřejmě rozhoduje již při formování v rámci operačního výkonu, ale další péče je také velmi důležitá. Po operaci se pahýl formuje bandážemi elastickým obinadlem do náležitého tvaru. Pahýl bandážujeme od vrcholu postupně proximálně tak, aby se snižoval pooperační otok a správně se pahýl formoval. Toto vyvazování naučíme nemocného. Později pahýl sprchujeme střídavě teplou a studenou vodou a kartáčujeme, abychom dosáhli obnovy kožní citlivosti.
Odborná rehabilitace začíná již první den pooperační kondičním cvičením na lůžku a po odstranění drénů pacienta mobilizujeme, jakmile to dovolí jeho celkový stav. Pacienta kontaktujeme s protetickým oddělením a spádovou rehabilitací. Motivujeme ho ve spolupráci s psychologem.
19.3 Komplikace amputací
Hematom je vážnou pooperační komplikací, která může vést k infekci, nekróze, bolestem. Větší hematom si většinou vyžádá revizi.
Nekróza
Dehiscence v ráně je méně častá. V jejím případě je indikována revize, toilleta a resutura.
Gangréna vzniká lokální ischemií, která může mít řadu příčin jako nevhodná úroveň amputace nebo arteriální uzávěr. Řešením je reamputace v optimální výši.
Edém je nejčastěji způsoben špatným obvazem či nešetrnou operační technikou. Následkem může být tzv. „hruškovitý pahýl“, který se obtížně protézuje.
Kontraktura vážně omezuje možnosti protézování a mobilizace pacienta.
Prevencí je správné polohování pahýlu a správná rehabilitace.
Bolest pooperační je samozřejmou součástí operačního výkonu a musíme ji pečlivě řešit analgetiky. Fantomové bolesti vznikají nejčastěji nesprávným ošetřením nervového pahýlu. Při jejich výskytu je třeba pokusit se řešit problém spoluprací s neurologem, psychologem a centrem bolesti. Pokud obtíže trvají, je po konzultaci s neurochirurgem nutná operační revize.
V oblasti pahýlu může dojít i ke zlomenině. Léčení je dle typu a lokalizace
Infekce je závažnou komplikací. Léčíme ji intenzivní ATB terapií dle citlivosti a především operační revizí se zavedením proplachové laváže nebo reamputací podle příčiny, mikrobiálního nálezu a celkového stavu pacienta.
Celkové komplikace:
Psychologické komplikace. Ztráta končetiny je u všech pacientů výrazným zásahem do života. Ne každý pacient je schopen tuto změnu akceptovat. Je nutná kvalitní rehabilitace a spolupráce s psychologem.
Morbidita a mortalita
U válečných poranění a polytraumat jsou samozřejmě vysoké. Snižuje je prevence šoku, dobrá chirurgická technika, první pomoc, dostupnost kvalitního ošetření a antibiotika. V mírových podmínkách je amputace při včasné indikaci a správném technickém provedení, relativně bezpečným výkonem.
19.4 Amputace u dětí
19.5 Typy amputací
Horní končetina
Na horní končetině provádíme intertorakoskapulární amputaci,exartikulaci v humeroskapulárním kloubu, amputaci v paži s pahýlem krátkým,středním nebo dlouhým. Dále jsou to exartikulace v lokti, amputace s dlouhým předloketním pahýlem, exartikulace v zápěstí a amputace v oblasti ruky.
Z amputací nazvaných podle autora na horní končetině známe především Krukenbergovu operaci. Jedná se o dlouhý předloketní amputační pahýl s podélným rozdělením mezi radiem a ulnou, který se přemění v klepeto s možností úchopu.
Dolní končetina
Na dolní končetině provádíme hemipelvektomii, exatrikulaci v kyčli, amputaci ve stehně s pahýlem krátkým, středním nebo amputaci s velmi dlouhým stehenním pahýlem. Dále jsou to exartikulace v koleně, amputace v bérci s pahýlem ultrakrátkým, krátkým, středním a amputace v oblasti hlezna a nohy.
Z amputací nazvaných podle autora na horní končetině známe především amputaci dle Scharpa, což je transmetatarzální amputace.
Amputace v Lisfrankově kloubu je oddělení všech kostí metatarzálních od kostí tarzálních.
Amputace dle Pirogova spočívá v odstranění všech kostí nohy s výjimkou dorzálních tří čtvrtin patní kosti, kterou se zachovalým úponem Achillovy šlachy překlopíme k upravenému distálnímu konci kosti holenní. Jde o nášlapný pahýl.
Amputace dle Symeho je odstranění všech částí nohy a distální části bérce těsně nad talokrurálním kloubem. Dlouhý dorzální kožní lalok je přetažen dopředu. Jde o nášlapný pahýl.
U amputace dle Callandera je vytvářen velmi dlouhý stehenní pahýl, u kterého je kostní amputace vedena ve výši kondylů femuru.
Amputace dle Stokes-Grittiho má stejně dlouhý kostní amputační pahýl jako amputace dle Callandera, ale zachovává se ventrální polovina čéšky, která se překlopí zespodu k femuru.
19.6 Protézování
Protézy dolních končetin
Protéza pro dolní končetinu se standardně skládá ze tří částí. Je to lůžko protézy (pahýlová objímka), trubková konstrukce a chodidlo.
Protézy dolních končetin je možno stavět dvěma způsoby. Klasická technologie stavby využívá kůži, kov, plsť a dřevo a protéza se připevňuje k tělu pomocí pásků a popruhů. Nyní se spíše užívají moderní technologie, jako jsou techniky podtlakového lití pryskyřičných plastů, vysokoteplotních i nízkoteplotních termoplastů a především užívání předem vyrobených dílů. Protéza je pak sestavována jako stavebnice z vysoce kvalitních, ale díky sériové výrobě výrazně levnějších dílů jako jsou klouby, konstrukce, chodidla či silikonové vložky.
Obr. 3: Pahýlový návlek bércový, který umožňuje správné nasazení protézy a chrání amputační pahýl (z propagačního materiálu firmy Sanomed)
Typy protéz
Sandálové protézy se užívají v případech amputací v Lisfrankově nebo Chopartově kloubu. Po aplikaci na nohu se obouvají do sériové nebo ortopedické obuvi.
Štítové protézy indikujeme v případech amputace ve vyšší oblasti nohy, jako jsou amputace dle Pirogova, Symea. Protéza se kryje punčochou a obouvá se do ortopedické obuvi.
Bércové protézy jsou jedny z nejčastěji konstruovaných a v moderním provedení pak umožňují vysoce kvalitní chůzi, bez kulhání.
Obr. 4: Bércová protéza (z propagačního materiálu firmy Sanomed)
Stehenní protézy se konstruují se speciálními kolenními klouby. Dříve měl kloub mechanickou západku, která umožňovala flexi po odjištění při sedu, ale na chůzi byl kloub fixován v extenzi. Nyní jsou již protézy vybaveny speciálními klouby umožňujícími chůzi.
Obr. 5: Stehenní protéza (z propagačního materiálu firmy Sanomed)
Obr. 6: Stehenní protézy připravené ke cvičení v Rehabilitačním ústavu Kladruby
Obr. 7: Moderní kloub nahrazující koleno u stehenní protézy
Protézy horní končetiny
Konstrukce protéz horní končetiny je odlišná od protéz dolní končetiny, jelikož neslouží k chůzi, ale k sebeobsluze a práci, kdy je spíše než pevnost požadována drobná motorika. Dříve se užívaly spíše epitézy, které měly jen kosmetickou funkci a byly dřevěné či pokryté PVC rukavicí vhodné barvy samozřejmě bez pohybu prstů. Pracovně se tento typ dá použít pouze k jednoduchému přidržování předmětů, jejich posouvání po podložce.
Vyšším stupněm jsou kosmetické protézy s mechanickou dlaní, která nahrazuje ruku jak kosmeticky, tak i částečně funkčně, jelikož umožňuje pasivní otevření dlaně např. druhou rukou a vložení předmětů do dlaně. V oblasti horní končetiny se stále častěji používají k obnově funkce ruky myoelektrické protézy, kdy se k iniciaci pohybu protézy, který je zajištěn elektromotoricky, využívají signály z daných svalových skupin. Můžeme tak dosáhnout provedení přesného pohybu jako je otevírání a zavírání dlaně, obě rotace v zápěstí či flexi a extenzi v loketním kloubu.
Obr. 8: Kosmeticky dokonalá protéza horní končetiny (z propagačního materiálu firmy Sanomed)
19.7 Rehabilitace po amputaci
20 Ošetřovatelský proces u pacienta s osteomyelitidou
20.3 Testovací otázky
20.1 Osteomyelitida
20.2 Septická artritida
21 Ošetřovatelský proces u pacienta s poraněním páteře
21.8 Testovací otázky
21.1 Úrazy páteře
21.1.1 Úrazy páteře bez poškození míchy
21.1.2 Úrazy páteře s poškozením míchy
21.2 První pomoc
21.3 Diagnostika
21.4 Léčba
21.4.1 Chirurgická léčba
21.4.2 Konzervativní léčba
21.4.3 Rehabilitace
21.4.4 Rehabilitační ošetřovatelství
21.4.5 Protetika
21.4.6 Rehabilitace následného období a sociální integrace
21.5 Prognóza
21.6 Komplikace
21.7 Nejčastější ošetřovatelské diagnózy
22 Ošetřovatelský proces u pacienta s úrazem mozku a míchy
22.1 Testovací otázky
Typy poranění, jejich diagnostika a léčba
23 Ošetřovatelský proces u pacienta s poruchou vědomí
23.6 Testovací otázky
23.1 Kvantitativní poruchy vědomí
23.2 Specifické kvantitativní poruchy vědomí
23.3 Glasgowská stupnice hloubky bezvědomí
23.4 První pomoc u pacienta v bezvědomí
23.5 Kvalitativní poruchy vědomí
24 Ošetřovatelský proces u pacienta s onemocněním prostaty
24.5 Testovací otázky
24.1 Benigní hyperplazie prostaty
24.2 Prostatitis
24.3 Karcinom prostaty
24.3.1 Základní vyšetření
24.3.2 Rozšířené vyšetření
24.4 Prevence
25 Ošetřovatelský proces u pacienta s nádorem plic
25.8 Testovací otázky
25.1 Rizikové faktory
25.2 Patologické formy karcinomu plic
25.2.1 Karcinom epidermoidní (z plochých buněk – skvamózní)
25.2.2 Adenokarcinom
25.2.3 Bronchoalveolární karcinom
25.2.4 Karcinom z velkých buněk (obrovskobuněčný karcinom)
25.2.5 Adeno-epidermoidní karcinom (adenoskvamózní)
25.2.6 Karcinoidy
25.2.7 Karcinomy z bronchiálních žlázek
25.2.8 Malobuněčný karcinom plic (karcinom z ovískových buněk)
25.2.9 Nemalobuněčný karcinom plic
25.3 Klinický obraz
25.4 Diagnostika
25.5 Rozvaha o operaci
25.5.1 Vzdálené metastázy
25.5.2 Nitrohrudní rozsev nádoru
25.5.3 Buněčný typ nádoru
25.5.4 Plicní a srdeční rezerva
25.6 Chirurgická léčba plicních nádorů
25.6.1 Důvody nízké operability
25.6.2 Indikace a kontraindikace chirurgické léčby
25.6.3 Onkologické kontraindikace
25.6.4 Somatické kontraindikace
25.6.5 Typy plicních operací
25.6.6 Rozšířené plicní výkony
25.6.7 Provedení lobektomie
25.6.8 Předoperační vyšetření
25.6.9 Funkční vyšetření plic
25.6.10 Předoperační příprava
25.6.11 Pooperační komplikace
25.6.12 Metastatické nádory plic
25.7 Transplantace plic
25.7.1 Historie
25.7.2 Indikační a kontraindikační kritéria k zařazení pacienta do transplantačního programu
25.7.3 Onemocnění indikovaná k transplantaci plic
25.7.4 Čekací listina
25.7.5 Dárce a odběr plic
25.7.6 Operace
25.7.7 Pooperační péče
25.7.8 Ambulantní péče
25.7.9 Rejekce
25.7.10 Závěr
26 Ošetřovatelský proces u gerontologického pacienta na chirurgickém oddělení
26.1 Testovací otázky
ASA I |
Zdravý pacient bez patologického klinického (psychosomatického) a laboratorního nálezu. Chorobný proces, jenž je indikací k operaci, je lokalizovaný a nezpůsobuje systémovou poruchu. |
ASA II |
Mírné až středně závažné systémové onemocnění, pro které je pacient operován, případně vyvolané jiným patologickým procesem (např. lehká hypertenze, diabetes mellitus, anémie, pokročilý věk, obezita, chronická bronchitida, lehká forma ICHS) |
ASA III |
Závažné systémové onemocnění jakékoli etiologie, omezující aktivitu nemocného (např. angina pectoris, stav po infarktu myokardu, závažná forma diabetu, srdeční selhání). |
ASA IV |
Závažné, život ohrožující systémové onemocnění, které není vždy operací řešitelné (srdeční dekompenzace, nestabilní angina pectoris, akutní myokarditida, pokročilá forma plicní, ledvinné, jaterní a endokrinní nedostatečnosti, hemoragický šok, peritonitis, ileus). |
ASA V |
Moribundní (umírající) nemocný, u něhož je operace poslední možností záchrany života. |
27 Ošetřovatelský proces u pacientky s karcinomem prsu
27.5 Testovací otázky